Природа - лиганд
Cтраница 2
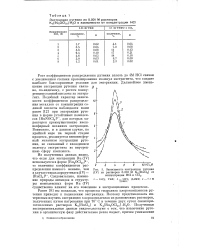 |
Зависимость экстракции рутения. [16] |
Следовательно, изменение природы лигандов и структуры комплексных форм Ru ( IV) существенно влияют на его поведение в экстракционных процессах. [17]
Данные о влиянии природы лигандов на частоты колебаний других актинил-ионов ( NpOg, PuOf, AmO и др.) в литературе представлены очень скудно. [18]
Зависимость величин Д от природы лигандов имеет регулярный характер, называемый спектрохимическим рядом, к рассмотрению которого мы теперь и перейдем. [19]
Что же касается влияния природы лигандов на каталитическую активность, это влияние ускоряет изомеризацию в двух случаях: 1) когда лиганд способствует переводу я-аллильного или а-комп-лекса в я-комплекс; 2) когда введение лиганда увеличивает скорость обмена комплекса с неизомеризованным олефином. [20]
Таким образом, влияние природы лигандов на каталитическую активность проявляется как на лимитирующей стадии, так и на стадиях, ей предшествующих. [21]
Из двух различных по природе лигандов, находящихся на лабилизованной оси, в первую очередь аквотируется лиганд с более сильным кристаллическим полем. [22]
Комплексные соединения классифицируются по природе лигандов или по характеру комплексных ионов. [23]
Как было указано [35], природа лигандов, присоединенных к иону металла, влияет а его жесткость и мягкость. По-видимому, жесткие лиганды делают лиганд еще - более жестким, а мягкие - более мягким по отношению ж дополнительным лигандам. Так, например, ионы металлов, связанные с серусодержащими лигандами или относительно мягкими порфириновыми кольцами, будут проявлять большую тенденцию к образованию комплексов с дополнительными мягкими лигандами по сравнению с гидратированньгм ионом металла [ М ( Н2О) 6 ] 2, связанным с молекулами воды, которые относятся к жестким лигаядам. Именно влиянием лягандов можно объяснить тот факт, что железо в теме столь прочно координирует такие мягкие лиганды, как СО и CN -, даже в присутствии большого количества жесткого лиганда воды. [24]
Энергия расщепления Д зависит от природы лигандов - и их расположения. [25]
Развивая мысль А. А. Гринберга о влиянии природы лигандов на окислительно-восстановительные свойства комплексного иона, мы пришли к выводу, что изучение равновесий комплексообразо-вания с позиций лиганда может оказаться особенно продуктивным. Действительно, при исследовании устойчивости комплексов оказывается, что индивидуальность центрального иона неизбежно нивелирует явления ступенчатой диссоциации; выбор комплек-сообразователей относительно ограничен; степени окисления их имеют определенные дискретные значения, равно как и потенциалы, характеризующие равновесия между смежными окисленными состояниями элемента. [26]
Гидролиз комплексов представляет собой изменение природы лигандов во внутренней сфере комплексов под действием воды. [27]
Гидролиз комплексов представляет собой изменение природы лигандов во внутренней сфере комплексов под. [28]
 |
Высокоспиновая и низкоспиновая структуры октаэдричес-кого комплекса с d6 - конфигурацией центрального иона. [29] |
Величина энергетического интервала А зависит от природы лигандов. В комплексах с лиган-дами, образующими прочные связи с катионом ( такие лиганды называются сильными), связывающие орбитали обладают очень низкой энергией, а разрыхляющие орбитали соответственно имеют очень высокую энергию ( см. разд. В этих случаях величина А имеет большое значение и образуются низкоспиновые комплексы. Примером сильного лиганда является цианид-ион. В случае слабых лигандов типа воды связывающие орбитали стабилизуются значительно меньше, а разрыхляющие орбитали дестабили-зуются также незначительно, и величина А оказывается небольшой. Это обусловливает образование высокоспиновых комплексов. [30]
Страницы: 1 2 3 4