Природа - лиганд
Cтраница 3
 |
Орби тали dz2 и dx - y в октаэдрическом поле. [31] |
Величина энергии расщепления Д зависит от природы лигандов и от конфигурации комплекса. [32]
Несколько слов следует сказать о влиянии природы лигандов и центрального атома на инверсионную нежесткость. [33]
Значительные усилия были потрачены на установление природы лигандов атома цинка до того, как стали известны трехмерная структура и аминокислотная последовательность КПА. [34]
В настоящее время мало сведений о природе лигандов, с которыми комплексуются ионы меди в белковой матрице лакказы. Кроме того, детальное исследование ЭПР-спект-ров лакказы показало, что одним из лигандов меди второго типа является вода, которая может быть замещена ионом фтора при ингибировании каталитической активности. [35]
Установлено, что на каталитическую активность влияет природа лигандов, причем полимеры обладают большей каталитической активностью, чем аналогичные мономерные хелаты или окислы металлов. Корреляция между каталитической активностью полимеров и их электропроводностью не установлена. [36]
Си ( II) сильно зависит от природы лигандов, и равновесие 2Си ( 1) ч Си ( 0) Cu ( II) может быть смещено в любом направлении в зависимости от условий. [37]
 |
Расщепление энергетического уровня d - орби-талей комплексообраэо-вателя воктаэдрическои поле лигандов. [38] |
Для данного комплексооб-разователя значение энергии расщепления определяется природой лигандов. [39]
Константа устойчивости и соответственно прочность комплекса зависит от природы лигандов и комплексообразователей, а также от значения координационного числа. В соответствии с теорией кислотно-основного взаимодействия ( см. § 8.3), ионы-комплексообразова-тели являются кислотами Льюиса, а лиганды - основаниями Льюиса. Все кислоты и основания разделены на два класса: жесткие и мягкие. К жестким кислотам относятся катионы, имеющие большое отношение заряда к радиусу, малую поляризуемость и не имеющие легко возбудимых электронов. К мягким кислотам относятся ионы, имеющие небольшое отношение заряда к радиусу, высокую поляризуемость и несколько легко возбудимых электронов. К ним относятся ионы - металлов VI и VII групп ( кроме хрома), железа, рутения, осмия, кадмия, семейства железа, а также ионы таллия, свинца и висмута. Промежуточное положение занимают ионы платины, палладия, иридия, родия, серебра, золота и ртути. К жестким основаниям относятся лиганды, донорные атомы которых находятся во втором периоде системы Д.И. Менделеева ( С, N, О, F), к мягким основаниям относятся остальные лиганды. Согласно правилу Пирсона жесткие кислоты предпочитают координировать жесткие основания, а мягкие кислоты - мягкие основания. [40]
 |
Расположение координатных осев в тетраэдря ческой комплексе. [41] |
Энергия расщепления Д энергетиче-с ких уровней зависит от природы лигандов и от конфигурации комплекса. Если лиганды и их расстояния от центра комплексообразователя одинаковы, то Д для тетраэдрического окружения комплексообразователя составляет 4 / 9 Д для октаэдрического окружения. [42]
С другой стороны, существенно сказывается также и природа лигандов, связанных с металлом. Если в той же реакции гидроцианирования моноцианидные комплексы ( имеют фрагмент - Cu ( Cl) CN) активны, то ди - и три-цианидные комплексы совершенно не активны. [43]
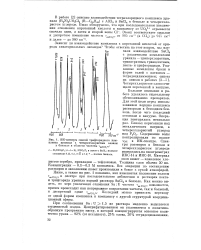 |
ИК-спектры смесей трифторидного ком. [44] |
Зависит ли взаимодействие комплекса с апротонной кислотой от природы экваториальных лигандов. [45]
Страницы: 1 2 3 4