Природа - растворитель
Cтраница 2
Природа растворителя может оказывать решающее влияние не только на скорость реакции, но и на ее тип, направление или стереохимию. [16]
Природа растворителя в реакциях Фриделя - Крафтса является чрезвычайно важным фактором. Воду и гидроксилсо-держащие растворители следует тщательно исключать, поскольку они реагируют с ацилирующим агентом и катализатором - кислотой Льюиса. Обычно растворителями служат нитробензол, нитроалканы, дисульфид углерода, простые эфиры или хлорированные углеводороды. Реакция протекает эффективнее, если катализатор растворим, но многие кислоты Льюиса, такие как хлорид алюминия, нерастворимы в реакционной среде, и тогда реакцию проводят в гетерогенной среде. Однако нитробензол и простые эфиры координируются с хлоридом алюминия и обеспечивают некоторую растворимость. Этилендихлорид является хорошим растворителем для комплексов ацилгалогенидов с хлоридом алюминия, так что избыток кислоты Лыоиса можно удалить фильтрованием; эта методика, известная как метод Перрье, позволяет при проведении ацилирования применять стехиометриче-ские количества ацилирующего агента и катализатора, причем субстрат прибавляют в последнюю очередь. [17]
 |
ИК-спектры исходного аниони - ra AH-25 ( а 0 ( / и закомплексованного ионами меди ( П в метиловом ( 2, этиловом ( 3 спиртах, ацетоне ( 4 и воде ( 5. [18] |
Природа растворителя особенно влияет на комплек-сообразующие свойства ионитов с гибкой полимерной матрицей и практически не оказывает влияния на свойства макропористых ионитов. В случае густосетчатых и макропористых ионитов такая замена значительно менее эффективна. [19]
Природа растворителя чаще всего не оказывает существенного влияния на процесс комплексообразования [9], во парафин получается различной степени чистоты [51, 52] ( см. стр. При выборе растворителя для процесса комплексообразования нужно учитывать его стоимость, дефицитность, токсичность, температуру кипения, испарения и другие факторы. [20]
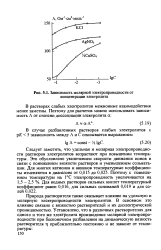 |
Зависимость молярной электропроводности от концентрации электролита. [21] |
Природа растворителя также оказывает влияние на удельную и молярную электропроводности электролитов. В основном это влияние связано с вязкостью растворителей и их диэлектрической проницаемостью. [22]
Природа растворителя оказывает существенное влияние на образование осадочных хроматограмм. Влияние природы растворителя определяется, с одной стороны, растворимостью в нем получаемых осадков, с другой - растворимостью в нем осадителя. [23]
Природа растворителя оказывает исключительно сильное влияние на процесс формирования пленки фоторезиста. Наиболее широко распространенным методом формирования пленки фоторезиста является метод центрифугирования. Данный метод состоит из двух этапов: нанесения на подложку определенной дозы светочувствительного раствора и получения необходимой толщины пленки за счет вращения ротора центрифуги с заданной скоростью. В некоторых случаях при формировании пленок фоторезистов наблюдается плохое смачивание ими поверхности подложек. Это явление устраняется механическим распределением фоторезиста по всей поверхности подложек, что обусловливает, однако, повышенную неравномерность формируемых пленок по толщине и увеличивает их загрязненность. [24]
Природа растворителя отражается и на клеящей способности связующего. Очень часто свойств одной только клеящей смолы бывает недостаточно для тех или иных целей; тогда для придания требуемых свойств в связующее вводятся различные добавки: пластификаторы, отвер-дители, ускорители, замедлители. [25]
Природа растворителя также влияет на активность катализатора. [26]
Природа растворителя сказывается не только при электролизе ацетатов. Довольно часто этот эффект наблюдается и при анодной конденсации моноэфиров дикарбоновых кислот. [27]
Природа растворителя оказывает очень сильное влияние на этот процесс, и степень ассоциации i зависит от природы растворителя и галогена X, но не R. [28]
Природа растворителя, как известно, сильно сказывается на свойствах растворенного вещества. Многосторонние исследования показали, что некоторые вещества, которые ведут себя как кислоты в среде одного растворителя, в другом растворителе проявляют себя как основания. Нередко в неводных растворах кислые или основные свойства проявляют такие вещества, которые, казалось бы, ничего общего не имеют с кислотами и основаниями в обычном представлении. [29]
Природа растворителя и температура играют основную роль. [30]
Страницы: 1 2 3 4