Природа - межмолекулярная сила
Cтраница 1
Природа межмолекулярных сил сложна и зависит от ряда - факторов. [1]
Изучение природы межмолекулярных сил, способствующих ассоциированию асфальтенов, является предметом многочисленных исследований. Обобщая имеющиеся сведения, можно объяснить стабилизацию надмолекулярной структуры асфальтенов, учитывая все виды взаимодействия, вносящие определенный вклад в суммарную энергию: а) дисперсионное, которое выражается в виде обмена электронами между однотипными неполярными фрагментами и действует на очень близких расстояниях ( 0 3 - 0 4 нм); б) ориентационное, которое проявляется в виде переноса зарядов между фрагментами, содержащими диполи или гетероатомы, также относится-к близкодействующим силам; в) я-взаимодействие ареновых фрагментов, формирующих блочную структуру; г) радикальное взаимодействие между неспаренными электронами молекул; д) взаимодействие за счет водородных связей гетероатомами и водородом соседних атомов составляющих е) взаимодействие функциональных групп, связанных водородными связями. [2]
Исследование природы межмолекулярных сил спектроскопическими методами основывается на изучении изменений полос поглощения и испускания при фазовых переходах, а также при замене растворителя. Различные типы связей проявляются неодинаково. Сравнительно часто наблюдаются сдвиги спектров, изменение их ширины, формы, интегральной интенсивности, появление новых полос или исчезновение старых. Содержащаяся в этих изменениях информация может быть расшифрована путем строгого и последовательного анализа, в процессе которого следует разделить спектроскопические эффекты, связанные с наличием разнообразных взаимодействий, и установить количественные соотношения между характеристиками спектральных полос и параметрами среды. [3]
Так как природа межмолекулярных сил, действующих внутри жидкости, изучена еще недостаточно хорошо, в настоящее время не имеется полезных для практики теоретических соотношений, связывающих А. [4]
Чтобы понять природу межмолекулярных сил, рассмотрим поведение нейтральных молекул в электрическом поле. Под действием электрического поля полярные молекулы вещества в той или иной степени ориентируются по направлению поля. Это явление называется ориентациоиной поляризацией. Тепловое движение стремится нарушить ориентацию молекул. В результате устанавливается некое равновесное состояние, зависящее от температуры и приложенного поля. [5]
XVII посвящена природе межмолекулярных сил в молекулярных кристаллах и обсуждению относящегося сюда экспериментального материала, включая материал, касающийся перехода от этого типа связи к другим типам. [6]
Сила межмолекулярного притяжения зависит от природы межмолекулярных сил, а также от расстояния между макромолекулами, причем чем расстояние меньше, тем сильнее взаимодействие между цепями. [7]
Связи между макромолекулами, независимо от природы межмолекулярных сил, намного слабее, чем химические ( валентные) связи, действующие вдоль макромолекулярных цепей. Этим объясняется возможность перемещения молекулярных цепей друг относительно друга, ориентации и дезориентации в зависимости от изменения температуры и действия внешних сил. [8]
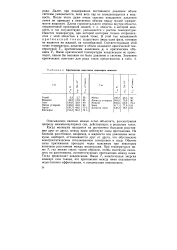 |
Критические константы некоторых веществ. [9] |
Описываемое явление можно легко объяснить, рассматривая природу межмолекулярных сил, действующих в реальных газах. [10]
Легко показать, что соотношение между указанными частотами определяется природой межмолекулярных сил, действующих на рассматриваемые молекулы в жидкой фазе. Действительно, если в исследуемом растворе преобладают силы универсального характера ( например, дисперсионные), то они должны, в соответствии с механизмом их действия ( взаимодействие мгновенных электронных осцилляторов) оказывать примерно одинаковое влияние на указанные колебательные частоты независимо от того, вращается молекула в сольвате или заторможена. [11]
 |
Расчет изменения свободной энергии. а-процесс, иллюстрирующий работу когезии. б-процесс, иллюстрирующий работу адгезии. [12] |
Оно не использует допущений, относящихся к молекулярной структуре или природе межмолекулярных сил притяжения, ответственных за адгезию. С другой стороны, это рассмотрение не дает сведений, касающихся силы, необходимой для разделения пары адгезивов, хотя это представляет значительный практический интерес. [13]
Понимание природы химической связи, обусловливающей образование молекул из атомов, кристаллических тел, а также природы межмолекулярных сил может быть достигнуто лишь на основании правильной, квантовомеханической модели атома, учитывающей волновые свойства электрона. [14]
Понимание природы химической связи, обусловливающей образование молекул из атомов, кристаллических тел, а также природы межмолекулярных сил южет быть достигнуто лишь на основании правильной, квантовомеханической модели атома, учитывающей волновые свойства электрона. [15]
Страницы: 1 2 3 4