Природа - межмолекулярная сила
Cтраница 4
Действительно, в случае атомов составляющие их элементарные объекты - ядра и электроны - были известны из опыта. Было также хорошо известно, что они связаны фундаментальным электромагнитным взаимодействием. Пользуясь им и известным фундаментальным электромагнитным взаимодействием, необходимо было также объяснить природу нефундаментальных межатомных и межмолекулярных сил, приводящих к образованию молекул и кристаллов. [46]
Так как энтальпии сольватации по порядку величины могут приближаться к энергиям связей ( 25 - 100 ккал / моль), растворитель во многих случаях следует рассматривать как участника реакции и включать его в уравнения реакций. Примером этого может служить выделение многочисленных сольватов, таких, как гидраты, алкоголяты, эфираты или аммиакаты преимущественно неорганических субстратов. Сольваты, образующиеся в результате межмолекулярного взаимодействия растворителя и субстрата, могут занимать между этими крайними случаями любое положение. Так как сольватация включает разнообразные силы взаимодействия, следует рассмотреть вопрос о природе межмолекулярных сил. [47]
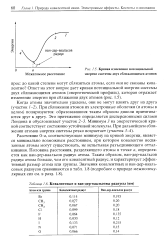 |
Кривая изменения потенциальной энергии системы двух сближающихся атомов.| Ковалентные и ван-дер-ваальсовы радиусы ( нм. [48] |
Расстояние 0-я, соответствующее минимуму на кривой энергии, является минимально возможным расстоянием, при котором ковалентно несвязанные атомы могут существовать, не испытывая разъединяющего отталкивания. Половина расстояния, разделяющего атомы в точке а, определяется как ван-дер-ваальсов радиус атома. Таким образом, ван-дер-ваальсов радиус атома больше, чем его ковалентный радиус, и характеризует эффективный размер атома или группы. Значения ковалентных и ван-дер-вааль-совых радиусов сравниваются в табл. 1.8 ( подробнее о природе межмолекулярных сил см. в разд. [49]
Особый вид связи наблюдается при взаимодействии атома водорода с сильно электроотрицательными элементами ( F, О, N, реже С1 и S), имеющими малые атомные радиусы. Так как в этой связи неизменно участвует водород, то она получила название водородной связи. Природа водородной связи в настоящее время до конца не выяснена. Некото рые исследователи считают, что ее природа ближе к природе межмолекулярных сил притяжения. Однако в действительности водородная связь не может быть сведена к ван-дер-ваальсовым силам, так как очевиден и ее электростатический характер. [50]
Страницы: 1 2 3 4