Природа - переходное состояние
Cтраница 3
Кинетический изотопный эффект при отщеплении протона от галоформа [ уравнение ( 2) ] представляет интерес в связи с природой переходного состояния. [31]
 |
Значения Ks и Ко при различных температурах.| Соотношение констант скорости и констант равновесия при различных составах спирто-водных смесей. Температура. С. 1 - 50. 2 - 60. 3 - 70. [32] |
Эти авторы указали, что имеется прямая связь между линейным соотношением энергии активации AG и свободной энергией реакции AG и природой переходного состояния. А именно, если угол наклона ( р) прямой АО L - AG близок к нулю, то переходное состояние имеет сходство с реагентами и процесс протекает по ассоциативному механизму. Если этот угол близок к единице, то переходное состояние имеет сходство с продуктами реакции и процесс протекает по диссоциативному механизму. Для определения величины р экспериментальные данные представлены на рис. 4 в координатах lg Ki - lg К. [33]
Здесь значение ( 3 фактически понижается от 0 9 до 0 4 с ростом кислотности кетона: такое значительное изменение необходимо связывать с изменением природы переходного состояния. [34]
Если начальное и конечное места миграции А и В в молекуле W-A-B-X хиральны, то стереохимия перегруппировки у атомов А и В будет зависеть от того, какова природа переходного состояния. В том случае, когда катион W-A-B достаточно стабилен и может некоторое время существовать в растворе как независимая частица, реализуется переходное состояние типа II или типа XVIII. Однако это справедливо лишь для молекул, строение которых не препятствует свободному вращению. [35]
По мере замещения атомов водорода в СН3С1, СН3Вг и СН31 на СН3, другие алкилы, фенильные и более объемные группы изменяются механизм, скорость реакции и природа переходного состояния. [36]
Хотя в 1935 г. Огг и Поляни [361] показали влияние сольватации на изменение потенциальной энергии при диссоциации молекул на ионы X Y - ( рис. 14), но они еще не представляли себе отчетливо природы переходного состояния, довольно ши роко пользуясь этим термином. [37]
Последние годы ознаменовались бурным развитием органической фотохимии для препаративного синтеза, что вызвало интерес к теоретическим проблемам, связанным с механизмом фотохимических реакций, Фотохимически возбужденная молекула во многом аналогична активированному комплексу, ее изучение может пролить дополнительный свет на природу переходного состояния. Для понимания фотохимических процессов следует рассмотреть две группы вопросов: первая относится к механизмам поглощения света молекулой, вторая - к дальнейшей судьбе этой энергии. [38]
Одно из ограничений и одна из полезных черт изо-кинетического соотношения состоит в том, - писал Леффлер - что, как можно полагать, оно приложимо лишь к тем сериям реакций, в которых растворитель или структурные изменения не меняют механизмы реакции или природу переходного состояния. [39]
Движущей силой реакции перегруппировки дипротонирован-ного гидразосоединения является электростатическое отталкивание двух близко расположенных положительных зарядов. Относительно природы переходного состояния последней стадии перегруппировки высказан ряд предположений. [40]
Хотя правило Прелога [13. 14], относящееся к асимметрическому синтезу атролактиновой кислоты, и правило Крама [15] сте-рического контроля асимметрической индукции в реакциях присоединения по карбонильной группе представляют собой детально разработанные эмпирические обобщения, основанные на опытных данных, возникает вопрос, в какой мере эти модели отражают действительный механизм этих реакций. Теоретические представления о природе переходных состояний в реакциях асимметрического синтеза являются полезными и весьма привлекательными. [41]
Относительные скорости не определяются одними изменениями, вызываемыми заместителями в свободной энергии переходного состояния. При рассмотрении проблемы реакционной способности природа переходного состояния столь же важна, как и природа исходных веществ. [42]
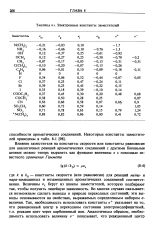 |
Электронные константы заместителей. [43] |
Величины тх берут из шкалы заместителей, которую подбирают так, чтобы получить линейную зависимость. Во многих случаях оказывается возможным сделать выводы о природе переходных состояний; эти выводы основываются на свойствах, выражаемых определенным набором а-величин. Так, необходимость использовать константы а4 указывает на то, что реакционный центр в переходном состоянии электронодефицитный, т.е. реакция идет через карбониевый ион. [44]
Другой пример касается электрофильного ароматического замещения. Эти реакции имеют отрицательные значения констант реакции р, что соответствует карбкатионной природе переходных состояний в таких реакциях. [45]
Страницы: 1 2 3 4