Притяжение - атом
Cтраница 1
Притяжение атомов С и атомов Н к атомам дублета деформирует связи в молекулах С2Н4 и Н2, приводит к их разрыву; в результате образуются новые связи, соответствующие продукту реакции. [1]
Притяжение атомов, являющееся результатом обобществления более чим одной нары электронов между двумя ядрами. При обобществлении двух пар ( одной а и одной л) образуется двойная связь. В том случае, если обобщены три пары электронов ( одна о и две я), образуется тройная связь. [2]
 |
Краевая дислокация, возникающая в результате сдвига. [3] |
Притяжение атомов примесей, вызванное разными причинами, приводит к осаждению этих атомов в виде цепочки вдоль края экстраплоскости. Такая цепочка инородных атомов называется атмосферой Коттрелла или облаком Коттрелла. С повышением температуры атмосфера Коттрелла рассасывается. При понижении температуры концентрация примеси около дислокации возрастает и по достижении предела растворимости вблизи ядра дислокации могут даже образоваться дисперсные выделения второй фазы. [4]
Стремление объяснить притяжение атомов друг к другу силами, подобными всемирному тяготению, натолкнулось на ряд затруднений. [5]
Адгезия обусловлена силами притяжения атомов, находящихся в разных фазах. [6]
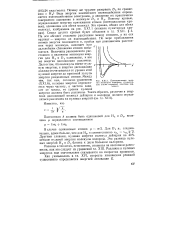 |
Потенциальная энергия молекулы водорода ( Пунктирные линии передают опытные значения. [7] |
Поэтому кривые, определяющие энергию притяжения атомов ( потенциальные кривые), одинаковы для обеих молекул. Эта кривая, общая для обеих молекул, изображена на рис. XXI. Смысл других кривых будет объяснен в гл. На оси абсцисс отложено расстояние между атомами, а на оси ординат - энергия их взаимодействия. По мере приближения атомов энергия понижается и, пройдя при равновесном расстоянии через минимум, начинает при дальнейшем сближении атомов повышаться. Величины равновесного расстояния и величины минимума энергии для Н2 и D2 одинаковы, и все же энергии диссоциации различны. Дело в том, что молекулы имеют нулевую энергию, и энергия диссоциации должна отсчитываться от уровня этой нулевой энергии до принятой за нуль энергии разделенных атомов. [8]
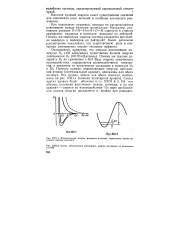 |
Потенциальная энергия молекулы водорода ( пунктирные линии передают опытные значения.| Схема, объясняющая зависимость энергии активации от изотопного состава. [9] |
Поэтому кривые, определяющие энергию притяжения атомов ( потенциальные кривые), одинаковы для обеих молекул. Эта кривая, общая для обеих молекул, изображена на рис. XXII. Смысл других кривых будет объяснен в гл. На оси абсцисс отложено расстояние между атомами, а на оси ординат - энергия их взаимодействия. [10]
Другой процесс сегрегации не связан с притяжением атомов углерода к структурным несовершенствам. При повышении температуры отпуска до 100 С эти кластеры укрупняются. [11]
Согласно Лондону доминирующий вклад в силу ван-дер-ва-альсова притяжения атомов, находящихся в основном состоянии, можно получить во втором порядке квантовомеханической теории возмущений в применении к оператору диполь-дипольного взаимодействия, причем энергия взаимодействия оказывается пропорциональной R-6. Расстояния, на которых лондоновское дисперсионное взаимодействие реально доминирует, относятся к области примерно от 5н - 8 А до 100 А. С уменьшением расстояния между атомами и приближением к ван-дер-ваальсову минимуму потенциала U ( R) ( см. рис. 1.1) следует учитывать также и другие вклады в энергию взаимодействия. [12]
Энергия обмена электронами между атомами ( энергия притяжения атомов) вносит основной вклад в энергию химической связи. [13]
Из табл. 5.11 и 5.12 видно, что притяжение атома примеси и вакансии ( Х-1) является главным фактором, обусловливающим зависимость теплоты переноса от концентрации. [14]
Электрон вылетает из катода в том случае, когда его энергии достаточно для преодоления притяжения атомов и отталкивания электронным облаком. Эта энергия измеряется так называемой работой выхода. [15]
Страницы: 1 2 3 4