Притяжение - атом
Cтраница 4
Однако обычных условиях, вследствие кулоновского расталкивания, невозможно достичь слияния ядер двух атомов. Значит, на каком-то расстоянии вместо притяжения атомов будет происходить их расталкивание. Таким образом, расстояние между атомами го, которому отвечает минимум на энергетической кривой, будет соответствовать длине химической связи, а энергия ECU - энергии связи. [46]
Первые вычисления энергии решеток длинноцепочечных парафинов были выполнены Мюллером. Сначала [202] Мюллер учитывал только энергию притяжения атомов, полагая, что отталкивание в кристаллической решетке не дает ощутимого вклада в энергию. [47]
По его мнению, существующее представление о так называемой двойной связи опровергается данными и физических и химических методов исследования. Так называемая двойная связь в действительности вызывает притяжение атомов более слабое, чем простая. Поэтому Брюль предлагает называть двойную связь одноненасыщенной связью, а тройную - двуненасыщенной [ там же, стр. [48]
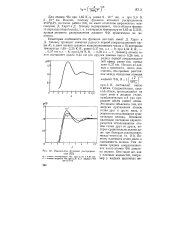 |
Радиальные функции распределения. [49] |
Следовательно, средний объем, приходящийся на один атом в жидком гелии, приблизительно в 6 раз превышает объем самого атома. Это можно объяснить тем, что энергия притяжения атомов гелия друг к другу мала, а энергия их отталкивания сравнительно велика. Основное квантовое состояние характеризуется отталкиванием атомов гелия друг от друга, которое сравнительно велико даже при больших расстояниях между ними ( см. гл. Поэтому плотность гелия мала, а сжимаемость велика. Тем не менее среднее координационное число атомов 4Не довольно велико. [50]
Некоторые указания на тип линейных комбинаций, которые следует ожидать, можно получить при рассмотрении молекулы: водорода. В этой молекуле концентрация электронов между ядрами обусловливает притяжение атомов друг к другу. Поэтому естественно предположить, что ряд линейных комбинаций, оказывающийся предпочтительным, дает волновые функции, каждая из которых сосредоточивается в некотором определенном направлении - в направлении образуемой связи - и дает наибольшую электронную плотность вдоль связи. На этом допущении и основываются соображения Паулинга. [51]
Хиггинс предполагал, что сущность химического сродства состоит в притяжении атомов. Но он пошел дальше и попытался для отдельных элементов выразить силу этого сродства количественно; в этом отношении большую услугу ему могли бы оказать данные его соотечественника и современника Кирвана, который установил зависимость между силой сродства кислот и оснований и количеством этих веществ, расходуемых при нейтрализации. [52]
Рассмотрим кристаллизацию насыщенных полимерных углеводородов, содержащих атомы углерода и водорода и не имеющих полярных групп. В каждый момент возникает асимметрия в распределении зарядов, обусловливающая притяжение атомов. Дисперсионные силы резко возрастают с уменьшением расстояния между макромолекулами. [53]
Бывает энергия химическая - энергия, высвобождаемая в химических реакциях. Упругая энергия в некотором роде похожа на химическую; и химическая энергия есть энергия притяжения атомов друг к другу, и упругая энергия тоже. [54]
Не следует думать, что эти схемы имеют буквальное значение. Изображение на плоскости тем более условно, что взаимное влияние атомов происходит в трехмерном пространстве и центры притяжения атома углерода равномерно распределены на его поверхности, которую для простоты можно принять за сферическую. Но такие плоскостные упрощенные, схематические формулы все-таки также необходимы, как, например, обычный плоский план какого-либо трехмерного здания. [55]
 |
Влияние строения заместителя в алкилгалогениде на изменение энергии активации и теплоты его реакции с атомом натрия 1392, стр. 23 ]. [56] |
Обобщив исследования, проведенные химиками с середины 30 - х до начала 40 - х годов XX в. Причем влияние заместителей может выражаться двояким образом: за счет изменения энергии отталкивания реагентов и за счет изменения энергии притяжения атомов в молекуле. [57]
Шаш [51] высказал предположение, что в этом случае обычным пространственным силам отталкивания между метильной группой и атомом галогена противодействуют электростатические силы притяжения атома X ( или группы С-X) и способной поляризоваться метильной группы, в результате чего у гош-формы имеется очень небольшой выигрыш в энергии. [58]
С помощью известных значений для п, а, В нетрудно проверить, что второе слагаемое в ( 41) не превышает 20 % от первого слагаемого. По абсолютной величине значение Um представляется вполне разумным, если иметь в виду, что у каждого атома имеется шесть ближайших соседей, а потенциал парного притяжения атомов имеет порядок величины нескольких градусов Кельвина. [59]
Страницы: 1 2 3 4