Дисперсионное притяжение
Cтраница 1
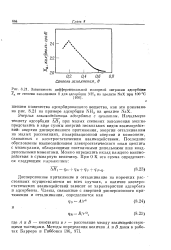 |
Зависимость дифференциальной молярной энтропии адсорбции Sa от степени заполнения 6 для адсорбции NH, на цеолите NaX при 100 С. [1] |
Дисперсионное притяжение и отталкивание на коротких расстояниях осуществляются во всех случаях, а наличие электростатических взаимодействий зависит от характеристик адсорбата и адсорбента. [2]
 |
Виды взаимодействия компонентов с неподвижной фазой в разных вариантах газовой и жидкостной хроматографии. [3] |
Дисперсионное притяжение имеет место в любом варианте хроматографии. [4]
Энергия дисперсионного притяжения убывает обратно пропорционально расстоянию в шестой степени. Таким образом, на достаточно больших расстояниях силы Лондона обеспечивают больший вклад в величину вандерваальсова взаимодействия, чем силы отталкивания. [5]
Константа дисперсионного притяжения С для многоэлектронных атомов может быть выражена через свойства взаимодействующих атомов с помощью различных приближенных квантово-механических формул. [6]
СО-А и ВО-А-константы дисперсионного притяжения и отталкивания для взаимодействия молекулы адсорбата с атомами кислорода решетки, CS-A. Даг - л - - тоже для взаимодействия молекулы адсорбата с катионом, LIJ - расстояния между центрами молекулы адсорбата и атомов кислорода решетки, а & К-А. Поляризационная энергия Фпол определялась из расчета напряженности электрического поля, создаваемого в центре молекулы адсорбата зарядом катиона и небольшими отрицательными зарядами, которые принимались равномерно распределенными по всем атомам кислорода решетки. [7]
Существенная трудность возникает при расчете константы дисперсионного притяжения С. [8]
В зависимости от соотношения величин энергии дисперсионного притяжения углеводородного радикала иона к поверхности адсорбента и энергии гидратации ионизированной группы адсорбированный ион ориентируется длинной осью параллельно поверхности раздела фаз либо под влиянием теплового движения ( и электростатического отталкивания), отрывающего от поверхности гидратированную полярную концевую группу иона, непрерывно изменяет свою ориентацию от параллельной до нормальной, как бы осциллируя вокруг углеродного атома радикала, наиболее удаленного от полярной группы и потому наиболее прочно закрепленного на поверхности адсорбента. [9]
Два значения вычислены с использованием для константы дисперсионного притяжения формул Лондона и Кирквуда - Мюллера. Поскольку первая формула обычно дает заниженную, а вторая завышенную величину, взято срздпее значение. [10]
 |
Значения коэффициента С8, отношения Cs / C6a02, равновесного расстояния г0 / ао и отношения С8 / С6г02 для атомов благородных газов. [11] |
При расчетах Ф полуэмпирический способ оценки параметров потенциала дисперсионного притяжения использовали особенно широко. Однако для параметров потенциала сил отталкивания квантовая механика не дает формул, аналогичных тем, которые она дает для параметров потенциала дисперсионного притяжения. [12]
Коагуляционные пространственные структуры образуются из свободнодисперсионных систем, когда дисперсионное притяжение между частицами преобладает над электростатическим отталкиванием. В этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского движения. [13]
Коагуляционные пространственные структуры образуются из свободнодисперсионных систем, когда дисперсионное притяжение между частицами преобладает над электростатическим отталкиванием. В этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского движения. [14]
 |
Виды контактов в пространственных дисперсных структурах. [15] |
Страницы: 1 2 3 4