Дисперсионное притяжение
Cтраница 2
Коагуляционные пространственные структуры образуются из свободнодисперсных систем, когда дисперсионное притяжение между частицами преобладает над электростатическим отталкиванием. В этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского движения. [16]
 |
Виды контактов в пространственных дисперсных структурах. [17] |
Коагуляционные пространственные структуры образуются из свободнодисперсионных систем, когда дисперсионное притяжение между частицами преобладает над электростатическим отталкиванием. В этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского движения. [18]
 |
Виды контактов в пространственных дисперсных структурах. а, б - коагу-ляционные с низкомолекулярны - § ми сольватными ( а и высокомолекулярными ( 5 слоями. в - точечные. г - фазовые контакты. [19] |
Коагуляционные пространственные структуры образуются из свободнодис-персных систем, когда дисперсионное притяжение между частицами преобладает над электростатическим отталкиванием. В этом случае энергия результирующего взаимного притяжения частиц сравнима с энергией их теплового броуновского движения. [20]
Как указано выше, шестая степень убывания потенциала моделирует электростатическое диполь-дипольное и дисперсионное притяжение. Двенадцатая степень убывания отталкивающего потенциала выбрана из соображений математического удобства. В то же время она моделирует достаточно жесткое отталкивание. При r - d потенциал равен нулю. Величина е характеризует глубину потенциальной ямы. [21]
Теплота включения может быть также вычислена по величине энергии дисперсионного притяжения и энергии отталкивания взаимодействующих молекул-гостей с водой. [22]
Энергия, рассчитанная таким образом, представляет собой сумму дисперсионного притяжения и отталкивания. [23]
Как сказано выше, квантовомеханические формулы для параметров сил дисперсионного притяжения и правила комбинирования для параметров сил притяжения и сил отталкивания являются приближенными. Поэтому для определения параметров функции ф, которые хорошо описывают экспериментальные значения К, а также позволяют их предсказывать, необходимо использовать экспериментальные адсорбционные данные. Так как на основании этих экспериментальных данных можно определить не более двух параметров, то в случае выбора теоретически более обоснованной модели потенциала ф, а также в слу-ч-ае адсорбции многоатомных молекул, когда число неизвестных параметров значительно больше двух, при использовании адсорбционных данных можно определить лишь часть этих параметров. В случае выбора для потенциала ф формы ( 6, 8, ехр) значения К наиболее чувствительны к погрешностям в значениях параметров С6 и г0 этого потенциала. [24]
Как было указано в первом разделе этой главы, параметры сил дисперсионного притяжения атом-атомных потенциалов межмолекулярного взаимодействия при адсорбции можно оценить, используя квантовомеханические формулы. Кроме того, параметры сил притяжения и сил отталкивания атом-атомных потенциалов межмолекулярного взаимодействия при адсорбции можно оценить с помощью правил комбинирования на основе соответствующих параметров атом-атомных потенциалов межмолекулярного взаимодействия молекул адсорбата друг с другом и силовых центров твердого тела друг с другом внутри кристаллической решетки. [25]
Учет корреляционных эффектов обязателен в расчетах межмолекулярных взаимодействий, так как важный эффект дисперсионного притяжения молекулярных систем с замкнутыми электронными оболочками имеет чисто корреляционную природу. [26]
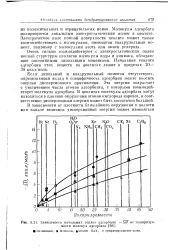 |
Зависимость начальных теплот адсорбции - ДЯ от поляризуемости молекул адсорбата. [27] |
Если дипольный и квадрупольный моменты отсутствуют, определяющий вклад в специфичность адсорбции может вносить энергия дисперсионного притяжения. Эта энергия возрастает с увеличением числа атомов адсорбента, с которыми взаимодействует молекула адсорбата. В цеолитах молекулы адсорбата могут находиться в плотном окружении атомов кислорода каркаса, и соответственно дисперсионная энергия может быть достаточно большой. [28]
А с любыми другими молекулами или адсорбентами ( в отсутствие химических реакций) обусловлены, в основном, универсальным неспецифическим дисперсионным притяжением. [29]
Эти атом-атомные потенциалы различаются как формой члена, аппроксимирующего потенциал сил отталкивания, так и числом членов описывающих потенциал сил дисперсионного притяжения. [30]
Страницы: 1 2 3 4