Дисперсионное притяжение
Cтраница 4
Исключая случай образования химических соединений, эти взаимодействия в основном обусловлены ван-дерваальсовскими силами, которые включают ориентационное притяжение между молекулами с постоянным диполем и молекулами с наведенным диполем, а также дисперсионное притяжение между молекулами со взаимно наведенными диполями. [46]
Из рассмотренных выше потенциалов теоретически наиболее обоснован потенциал ( VIII16) Бакингема - Корнера ( 6 8, ехр), в котором для сил отталкивания принято экспоненциальное выражение, а для сил дисперсионного притяжения учтены первые два члена мульти-польного разложения энергии этих сил. В потенциале Бакингема ( 6, ехр) учтен только один первый член этого разложения, а в потенциале Леннард-Джонса ( 6 12) и аналогичных ему потенциалах ( 6 п) ( где п - показатель степени в члене Вг - п), кроме того, для сил отталкивания вместо экспоненциального члена эмпирически принят степенной. [47]
Из теории возмущений следует, что энергию взаимодействия двух молекул можно представить в виде суммы, в которой первое слагаемое в случае вандерваальсового взаимодействия двух неполярных молекул представляет энергию отталкивания, а второе слагаемое - энергию дисперсионного притяжения ( кулоновский член второго порядка) и обменную энергию второго порядка. Поэтому обычно вкладом последнего члена пренебрегают, и энергию взаимодействия двух молекул в области потенциального минимума представляют в виде суммы энергии отталкивания и энергии дисперсионного притяжения. [48]
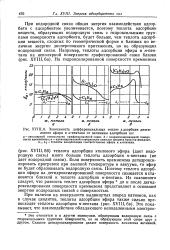 |
Зависимость дифференциальных теплот адсорбции диэти-лового эфира и н-пентана от величины адсорбции на. [49] |
При водородной связи общая энергия взаимодействия адсор-бата с адсорбентом увеличивается, поэтому теплота адсорбции веществ, образующих водородную связь с гидроксильными группами поверхности адсорбента, будет больше, чем теплота адсорбции веществ, сходных по геометрической форме и близких цо величине энергии дисперсионного притяжения, но не образующих водородной связи. [50]
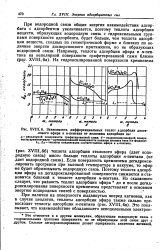 |
Зависимость дифференциальных теплот адсорбции диэти-лового эфира и н-пентана от величины адсорбции на. [51] |
При водородной связи общая энергия взаимодействия адсор-бата с адсорбентом увеличивается, поэтому теплота адсорбции веществ, образующих водородную связь с гидроксильными группами поверхности адсорбента, будет больше, чем теплота адсорбции веществ, сходных по геометрической форме и близких по величине энергии дисперсионного притяжения, но не образующих водородной связи. [52]
Дисперсионная составляющая притяжения молекул универсальна и п рисут-ствует всегда. Наиболее отчетливо дисперсионное притяжение проявляется при взаимодействии неполярных молекул и взаимодействии атомов благородных газов. Эти силы сравнимы по величине с силами полярных межмолекулярных взаимодействий. Суть возникновения дисперсионных сил заключается в следующем. При движении электронов в молекуле мгновенно возникает асимметрия распределения положительных и отрицательных зарядов. [53]
Страницы: 1 2 3 4