Межмолекулярное притяжение
Cтраница 1
Межмолекулярное притяжение, действующее в местах контакта трущихся тел. Сейчас важно усвоить одно - между молекулами вещества на очень малых расстояниях возникает притяжение. [1]
 |
Схема возникновения дисперсионных сил взаимодействия между двумя частицами на модели атома водорода. [2] |
Межмолекулярное притяжение, обусловливаемое ван-дер-ваальсовыми силами, представляет собой одно из общих явлений природы. Оно свойственно всем веществам и проявляется в газе - и парообразном, жидком и твердом его состояниях. Как мы видели, межмолекулярное когезионное взаимодействие лежит в основе агрегатного состояния вещества при данных физических условиях. [3]
Межмолекулярное притяжение не исчерпывается ориентационны-ми и индукционными взаимодействиями. Известно большое количество веществ, таких, как, например, благородные газы, молекулы которых неполярны и относительно мало поляризуются. И тем не менее эти вещества получены как в жидком, так и в твердом состояниях. Он показал, что электростатическое отталкивание между электронами двух каких-либо атомов или молекул уменьшается, если движение электронов происходит таким образом, что они все время оказываются максимально удаленными друг от друга. [4]
Межмолекулярное притяжение, обусловливаемое силами Ван-дер - Ваальса, представляет собой одно из всеобщих явлений природы. Оно свойственно всем веществам и проявляется в газо - и парообразных, жидком и твердом его состояниях и лежит в основе агрегатного состояния вещества при данных физических условиях. [5]
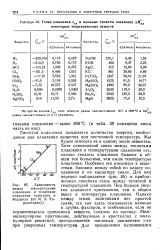 |
Точки плавления fnj ] и мольные теплоты плавления ДЯПЛ некоторых неорганических веществ. [6] |
Межмолекулярное притяжение, действующее в кристаллах с молекулярной решеткой, преодолевается тепловым движением уже при умеренных температурах. [7]
Межмолекулярное притяжение не исчерпывается ориентаци-онными и индукционными взаимодействиями. Известно большое число веществ, таких, как, например, благородные газы, молекулы которых неполярны и относительно мало поляризуются. И тем не менее эти вещества получены как в жидком, так и в твердом состояниях. Он показал, что электростатическое отталкивание между электронами двух каких-либо атомов или молекул уменьшается, если движение электронов происходит таким образом, что они все время оказываются максимально удаленными друг от друга. При таком согласованном движении электронов каждый из атомов можно рассматривать как мгновенный электрический диполь, положительный полюс которого расположен в ядре атома, а отрицательный - в точке нахождения данного электрона. При согласованном движении электронов такие мгновенные диполи ориентируются друг к другу противоположно заряженными концами, в результате чего происходит их электростатическое притяжение. [8]
Учитывая межмолекулярное притяжение, Фрумкин нашел более сложное выражение для зависимости а а ( с), которое справедливо и для больших концентраций поверхностпоактивпого компонента. [9]
Силы межмолекулярного притяжения, действующие между электрически нейтральными частицами и являющиеся причиной появления постоянной а в уравнении Ван-дер - Ваальса, получили название силы Ван-дер - Ваалъса. [10]
Энергия межмолекулярного притяжения не ограничивается слагаемыми Uop, t / инд. Для таких неполярных веществ, как Ne и Аг, оба этих слагаемых равны нулю, тем не менне благородные газы сжижаются, что свидетельствует о наличии еще одной составляющей межмолекулярных сил. [11]
Наличие межмолекулярного притяжения равносильно добавочному давлению, прижимающему молекулы друг к другу. Значит, вместо р нужно писать р рвн, где РВН - добавочное внутреннее давление в газе. Оно, очевидно, зависит от объема: чем меньший объем занимает газ, тем больше силы межмолекулярного притяжения. [12]
Наличие межмолекулярного притяжения равносильно добавочному давлению, прижимающему молекулы друг к другу. Значит, вместо р нужно писать р рвн, где уОвн - добавочное внутреннее давление в газе. Оно, очевидно, зависит от объема: чем меньший объем занимает газ, тем больше силы межмолекулярного притяжения. [13]
Силы межмолекулярного притяжения очень быстро убывают с увеличением расстояния между частицами. Поэтому можно считать, что они проявляются лишь в областях действительного контакта между телами. [14]
Сила межмолекулярного притяжения зависит от природы межмолекулярных сил, а также от расстояния между макромолекулами, причем чем расстояние меньше, тем сильнее взаимодействие между цепями. [15]
Страницы: 1 2 3 4