Термодинамическая причина
Cтраница 1
Термодинамическая причина связана с тем, что вследствие сильной интерференции упругих полей дислокаций в энергию ансамбля дефектов основной вклад дает энергия взаимодействия. Поэтому при некоторой критической плотности рс силы взаимодействия между дислокациями становятся больше внешних сил, требуемых на преодоление сопротивления при движении отдельного дефекта в бездислокационной решетке. Тогда независимые перемещения отдельных дислокаций становятся невозможными. [1]
Кроме термодинамических причин ( прочность химических связей) существуют также кинетические причины. [2]
По термодинамическим причинам каждая электрохимическая реакция может протекать только в определенной области потенциалов: катодная реакция - при потенциалах электрода отрицательнее, анодная реакция-при потенциалах положитель-нее равновесного потенциала данной реакции. Это условие означает только возможность протекания электродной реакции в соответствующей области потенциалов, но ничего не говорит о том, протекает ли реакция на самом деле и какова ее скорость. Ответы на эти вопросы даются не термодинамикой, а электрохимической кинетикой. [3]
 |
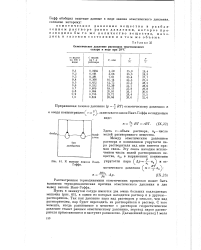
Связь между энергией активации и предэкспоненциальным множителем для реакции окисления изооктана и циклогексана ( по данным С. 3. Рогинского. [4] |
По статистическим и термодинамическим причинам они должны быть тем более многочисленны, чем ниже их энергия. Увеличение числа активных центров соответствует увеличению значения Z. В то же время активные центры должны быть тем менее эффективны, чем. [5]
Были найдены термодинамические причины отклонения равновесного распределения от распределения Флори в случае разбавленных [19] и концентрированных растворов. [6]
II были рассмотрены термодинамические причины, обусловливающие термическую стойкость полимерных соединений. Ниже обсуждается кинетика некоторых процессов деструкции полимеров. [7]
По той же термодинамической причине углерод чугуна в сталеплавильной ванне окисляется только до окиси углерода, создавая восстановительный режим для расположенной выше шлаковой фазы. [8]
Уточним, в чем заключаются термодинамические причины возникновения различия компонентов. [9]
Их регуляторное действие может быть обусловлено прямыми термодинамическими причинами, как в случае с концентрацией Н2 - Практически не рассмотрены сигнальные пути в сообществе, например, под воздействием физиологически активных веществ. Причина состоит в том, что сигнальные пути в большинстве видоспецифичны, как например, для антибиотиков. Но главное состоит в том, что они вступают в действие, когда выполнены перечисленные выше трофические требования. [10]
 |
К выводу закона Вант - упругости пара ( Др - - п2 и ос - Гоффа. ч, 1 д. [11] |
Рассмотрением термодинамики осмотических процессов может быть выяснена термодинамическая причина осмотического давления и дан вывод закона Вант-Гоффа. [12]
В работе автора [1] указано на существование термодинамических причин явлений перенапряжения в электрохимических реакциях. Одновременно установлены общие термодинамические зависимости перенапряжения от природы металла. Предсказанная на основе термодинамического рассмотрения связь между химическим потенциалом электронов в металле и перенапряжением действительно наблюдается в процессах электролитического выделения водорода из водных и из спиртовых растворов, а также в процессах катодного восстановления кислорода, в процессах электролитического выделения кислорода из водных растворов и в др. процессах. Представляется целесообразным использовать также кинетический подход для установления связи между перенапряжением водорода и природой металла. Нам представляется, что для этой цели может быть полезным применение некоторых положений мультиплетной теории катализа, развитой академиком Баландиным и оказавшейся весьма плодотворной для понимания результатов многих каталитических реакций. Естественно предполагать, что водородные атомы, возникающие в процессах разряда водородных ионов на электроде, являются адсорбированными и деформированными. В соответствии с мультиплетной теорией можно предположить, что радиус деформированного водородного атома, находящегося на поверхности металла, равен атомному радиусу металла. [13]
Вероятно, формирование триазольного цикла более предпочтительно по термодинамическим причинам по сравнению с образованием производного [1.2.4] триазола. [14]
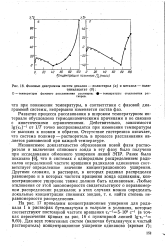 |
Фазовые диаграммы систем декалин - полистирол ( а и метанол - поли. [15] |
Страницы: 1 2 3 4