Термодинамическая причина
Cтраница 3
С увеличением температуры растворимость газа в жидкости, как правило, уменьшается. Термодинамической причиной этой зависимости является выделение теплоты гидратации ( сольватации) молекул при растворении. Согласно принципу смещения равновесия, экзотермический процесс сдвигается в сторону поглощения теплоты, а следовательно, уменьшается растворимость газа. Чистые жидкости легко образуют с газом пересыщенные растворы. Пересыщение легко устраняется введением в раствор твердых частиц или пузырьков газа, образующихся при кипячении. [31]
 |
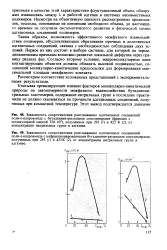
Изотермы сорбции и соответствующие их хро-матограммы. [32] |
Искажение хроматографических пиков мешает эффективной работе колонки и точному определению характеристик удерживания. Для устранения термодинамических причин размывания и асимметрии хроматографических пиков подбирают адсорбенты, дающие линейную изотерму, или добиваются большей линейности благодаря термическому, химическому или физическому модифицированию носителя. [33]
Этот факт объясняется термодинамическими причинами. [34]
Рассмотрим процесс образования триоксана из водного раствора формальдегида. Этот факт легко объясняется термодинамическими причинами. [35]
В чем же состоит идея термодинамического подхода. Тогда образование ряда структур запрещено по термодинамическим причинам и образующийся полимер будет иметь определенную структуру. [36]
Рассмотрим, в первую очередь, наиболее важные для структурной химии реконструктивные превращения. Вообще, изменение структуры и объема вещества всегда происходит вследствие термодинамических причин в соответствии с диаграммой состояния вещества. Однако кристаллохимия позволяет избежать запоминания многочисленных фактов, поскольку при повышении давления всегда увеличивается степень заполнения пространства, а уменьшение давления делает стабильной более рыхлую структуру. Поскольку рост КЧ приводит к более плотной упаковке атомов, реконструктивный ФП при высоком давлении всегда повышает координацию атомов. [37]
Ввиду этого нужно какое-либо воздействие, чтобы скомпенсировать вредное по термодинамическим причинам ( но полезное по кинетическим) влияние высокой температуры. Течение данной реакции слева направо сопровождается уменьшением количества вещества ( моль) ( Av-2), следовательно, давление оказывается благоприятным фактором. [38]
Однако прямой корреляции между содержанием этих групп и термодинамическими свойствами поверхности не наблюдается. Авторами работы было сделано предположение о том, что в силу термодинамических причин активные функциональные группы, образовавшиеся в процессе облучения, не остаются на поверхности, а уходят с нее в приповерхностный слой. [39]
 |
Зависимость значений QBH ( 1, QS M ( 2 и АН ( 3 для платинированной платины от потенциала. [40] |
Вид изотермы обусловлен уменьшением теплоты адсорбции ge по мере роста степени покрытия электрода. Разряд ионов водорода с образованием молекулярного ( газообразного) водорода по термодинамическим причинам возможен только при потенциалах, отрицательнее О В. [41]
Таким образом, возможность эффективного межфазного взаимодействия полимеров, обусловливающая образование прочных и долговечных адгезионных соединений, связана с необходимостью соблюдения двух условий. Первое из них состоит в выборе системы, для которой по термодинамическим причинам возможно развитие локальной диффузии через границу раздела фаз. Согласно второму условию, макромолекулярные цепи контактирующих объектов должны обладать высокой подвижностью, создающей молекулярно-кинетические предпосылки для формирования максимальной площади межфазного контакта. [43]
Таким образом, ионы хлора в щелочном растворе активируют железо, на поверхности которого имеется фазовый окисный слой или только адсорбированный пассивирующий кислород. Активация наступает при достижении некоторого, достаточно положительного потенциала, при котором ионы хлора по термодинамическим причинам далеко еще не могут окисляться до молекул СЬ, но, конечно, могут образовывать соединение с железом, вытесняя кислород ( или гидроксил) из железного окисла. Очевидно, в случае адсорбционной пассивности механизм активации может быть только адсорбционным и положительный потенциал необходим для того, чтобы могла осуществиться хемосорбция хлора на железе. [44]
Помимо межвидовой конкуренции за доминирование в пределах одной экологической ниши, существует конкуренция между группами организмов в пределах сообщества. Уже упоминалось, что предпочтение между акцепторами электрона для одних и тех же доноров определяется термодинамическими причинами с использованием в первую очередь реакций, дающих наибольший энергетический выигрыш. Наглядно этот тип конкуренции можно рассмотреть на уже неоднократно обсуждавшемся примере конкуренции между сульфидогенами и меташгенами, как это было сделано В. А. Вавилиным на основе данных микробиологов для очистных сооружений, где процесс идет в контролируемых условиях в очень большом масштабе. [45]
Страницы: 1 2 3 4