Ван-дро
Cтраница 1
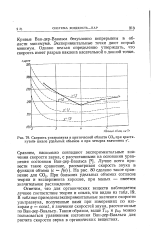 |
Скорость ультразвука в критической области СО2 при растянутой шкале удельных объемов и при четырех значениях г. [1] |
Кривые Ван-дер - Ваальса безусловно непрерывны в области минимума. [2]
Уравнение Ван-дер - Ваальса может быть получено из уравнения Клапейрона-Менделеева внесением поправки а / У2 к давлению и поправки b к объему. [3]
Силы Ван-дер - Ваальса - относительно слабые, они действуют между насыщенными молекулами и отдельными атомами, не имеющими свободных валентных связей, не являющимися жесткими диполями и не содержащими перманентных диполей. Они действуют между атомами инертных газов Не, Ne, Ar, Хе, Кг, молекулами трудно сжимаемых газов N2, Оа, СО и СН4 и между всеми неполярными органическими молекулами в жидкостях и твердых телах. Хар-кинс предложил приводимое ниже объяснение природы сил Ван-дер - Ваальса, позволяющее понимать их характер. На относительно больших расстояниях для больших промежутков времени молекулы взаимодействуют друг с другом так, как если бы они были симметричны, но мгновенно и на меньших расстояниях взаимодействовали как диполи за счет перманентно возникающих недостатков симметрии в электронной системе. Такой атомный диполь индуцирует поляризацию в смежном атоме. [4]
 |
Изотермы углекислого газа, полученные Эндрюсом. [5] |
Уравнение Ван-дер - Ваальса в критической области удовлетворительно описывает состояние жидкостей и газов как качественно, так и количественно. Однако в области температур ниже критической оно дает для жидкостей только качественное описание состояния системы. [6]
Силы Ван-дер - Ваальса имеют электрическую природу и обусловлены взаимодействием между собой молекул с мгновенными диполями, возникающими в неполярных молекулах ( дисперсионный эффект), а также с постоянными индуцированными диполями. Следует указать на аддитивность ван-дер-ваальсрвых сил ( точнее большей части из них), вследствие чего - энергия притяжения поверхностью, состоящей из многих молекул, значительно больше и убывает с расстоянием медленнее, чем энергия взаимодействия отдельных молекул между собой. [7]
Работа Ван-дер - Ваальса ясно показала, что для водорода эффект Джоуля - Томсона наблюдается только после того, как температура его снизится ниже некоторого определенного значения. И чтобы снизить температуру водорода до требуемого значения, перед проведением цикла расширения газ следует охладить. [8]
Силы Ван-дер - Ваальса складываются из следующих сил взаимодействия: ориентационных, индукционных и дисперсионных. [9]
 |
Физические постоянные некоторых газов. [10] |
Уравнение Ван-дер - Ваальса с качественной стороны достаточно хорошо описывает свойства реального газа, но результаты численных расчетов не всегда согласуются с экспериментальными данными. В ряде случаев эти отклонения объясняются склонностью молекул реального газа к ассоциации в отдельные группы, состоящие из двух, трех и более молекул. [11]
 |
Кристалл иода, образованный из отдельных двухатомных молекул г. Молекулы, изображенные прерывистыми линиями, находятся под плоскостью, в которой лежат молекулы, изображенные сплошными линиями. [12] |
Силы Ван-дер - Ваальса имеют ненаправленный характер, вследствие чего молекулы располагаются по возможности тесно. В такой плотной кубической упаковке каждый атом имеет двенадцать ближайших соседей. Аналогичная упаковка осуществляется в кристаллах НС1, HBr, H2S, CH4; в большинстве подобных систем при температурах, не слишком далеких от точки плавления, отдельные молекулы могут вращаться. Если, как в случае бензола, форма молекулы весьма отличается от сферической, упаковка все же такова, что у каждой отдельной молекулы имеется максимально возможное число соседей. [13]
Уравнение Ван-дер - Ваальса известно с последней четверти прошлого века. Но не надо спрашивать, почему не вычислили парциальных мольных объемов по уравнению Ван-дер - Ваальса гораздо раньше и уже давно не обнаружили их своеобразия вблизи критической точки чистого растворителя. Не экспериментируют и не вычисляют без идей, а идеи о необычности свойств бесконечно разбавленных растворов в окрестности критической точки чистого растворителя не существовало. Предсказать дату возникновения идеи ( пока) никто не умеет. [14]
Уравнение Ван-дер - Ваальса при температурах ниже критической и объемах, меньших 0 3 м3 клголь 1 дает неверные результаты. Поэтому расчет свойств реальных газов при таких условиях производят другим путем. [15]
Страницы: 1 2 3 4