Уравнение ван-лаара
Cтраница 1
Уравнения Ван-Лаара могут удовлетворительно описывать системы с высокими значениями величин ААВ и АВА и более несимметричные, чем системы, характеризуемые уравнениями Маргулеса. Однако к системам с очень большими отношениями АВА / АЛВ уравнения Ван-Лаара не применимы. В тех случаях, когда отношение АВА / ААВ близко к двум, уравнения Ван-Лаара лучше соответствуют опытным данным по сравнению с уравнениями Маргулеса. [1]
Применимость уравнений Ван-Лаара для описания условий фазового равновесия в системах рассматриваемого типа была проверена на примере системы этиловый спирт - вода - нитрат калия. [2]
В уравнениях Ван-Лаара характер связи избыточных термодинамических функций с составом иной, чем в двухпараметри-ческих уравнениях Маргулеса и Редлиха - Кистера: уравнение ( VII. Последнее и определяет область применимости уравнений Ван-Лаара. [3]
Наиболее простыми являются уравнения Ван-Лаара и Маргулеса с двумя константами. При А В из уравнений Ван-Лаара и Маргулеса получаются уравнения, выражающие зависимость коэффициентов активности от состава для регулярных растворов ( см. уравнения 139, стр. Из уравнений ( 223) вытекает линейная зависимость логарифма отношения коэффициентов активности от состава; благодаря своей простоте, эти уравнения получили применение при рассмотрении некоторых вопросов теории растворов. [4]
Наиболее простыми являются уравнения Ван-Лаара и Маргулеса с двумя константами. При А В из уравнений Ван-Лаара и Маргулеса получаются уравнения, выражающие зависимость коэффициентов активности от состава для регулярных растворов ( см. уравнения 139, стр. Особенностью последних уравнений является то, что зависимость коэффициентов активности обоих компонентов от состава выражается симметричными кривыми. Из уравнений ( 223) вытекает линейная зависимость логарифма отношения коэффициентов активности от состава; благодаря своей простоте, эти уравнения получили применение при рассмотрении некоторых вопросов теории растворов. [5]
Для определения констант в уравнениях Ван-Лаара второго порядка кроме конечных величин при хА 0 и 1 0 имеется сравнительно мало промежуточных точек ( л А 0 5 и lgYA / Ys 0) - Однако для систем с положительными отклонениями от закона Рауля применимость уравнений Ван-Лаара можно установить на основе зависимости ( IgYA) 0 5 от ( IgYs) 0 5 которая в этом случае должна быть прямолинейной; кроме того, на оси ординат и оси абсцисс должны отсекаться отрезки, равные соответственно А АВ и ABA - В случае симметричных уравнений с одной константой зависимость на рис. 49 будет изображаться прямой линией. [6]
Кривые igy - полученные из уравнений Ван-лаара или каким-либо иным методом интегрирования уравнения Дюгема, будут также полезны для сглаживания и интерполирования экспериментальных данных в этой области. [7]
При подстановке этих коэффициентов активности в уравнения Ван-Лаара или Маргулеса получаются системы двух уравнений с двумя неизвестными, которые могут быть решены относительно констант. [8]
Анализ формы геометрических кривых, описываемых уравнением Ван-Лаара, показывает, что они на диаграмме плавкости в области неограниченного смешения в жидкой и твердой фазах имеют монотонный вид с выпуклостью, обращенной вверх или вниз. Если образующееся химическое соединение недиссоциировано в жидком и твердом состояниях, его можно рассматривать как компонент. На диаграмме плавкости двойной системы фигуративная точка его окружена слева и справа сплавами. Ликвидус от точки плавления соединения может транслироваться налево в сторону компонента А и направо к компоненту В в виде кривых, форма которых регламентирована уравнением Ван-Лаара. [9]
 |
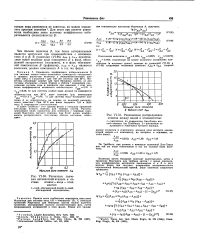
Зависимость коэфициентов активности, вычисленных по уравнению Ван-Лаара, от мольных долей. [10] |
Типичные кривые активности легко можно найти из уравнений Ван-Лаара подбором значений АН В. Кривые, приведенные на рис. 133 ( взяты из статьи Карлсона и Колборна) и основанные на значениях А 1 13 и В 0 49, очень хорошо воспроизводят данные по системе н-пропиловый спирт - вода при 1 атм. [11]
Если система образует азеотроп, то коэффициенты уравнений Ван-Лаара А и В могут быть вычислены по температуре кипения и составу азеотропа. [12]
При расчете коэффициентов активности водных растворов рекомендуется использовать уравнения Ван-Лаара, Вильсона, Цубоки - Катаямы, а также современные версии моделей групповых вкладов и др. Обращаем внимание на трудности в некоторых случаях корректного определения температурных зависимостей коэффициентов активности. [13]
Встречаются также уравнения, основанные на симметричной форме уравнения Ван-Лаара. [14]
 |
ЗО. Расчетные значения активностей этанола в системе этанол - вода - этил-ацетат.| Равновесное распределение этанола между водой и этилацетатом. [15] |
Страницы: 1 2 3 4