Уравнение ван-лаара
Cтраница 3
Вычислим равновесие жидкость - пар для системы метанол - бензол, пользуясь уравнениями Ван-Лаара. Константы уравнения вычисляют на основании данных для азеотропной смеси, образующейся в этой системе, хотя можно использовать данные: и для любой другой точки системы. Метанол и бензол образуют азеотроп, кипящий при 57 5 ( при общем давлении 760 мм рт. ст.) и содержащий 61 0 % мол. [31]
Показано, что экспериментальные и расчетные данные, полученные на основании выполненного решения уравнения Ван-Лаара хорошо согласуются между собой. Это позволяет применить решение уравнения для расчетного определения составов паровой фазы и температуры при построении диаграммы равновесия. [32]
Выражения ( 12 - 88) и ( 12 - 89) называются уравнениями Ван-Лаара. [33]
Уравнения ( 9) и ( 10) иногда называют не совсем правильно уравнением Ван-Лаара. Ван-Лаар действительно вывел уравнения для изменения энтальпии, но на основании совершенно других предположений об аналогии между жидкостью и реальным газом. В константу В в уравнении Ван-Лаара входят постоянные аг и аг уравнения Ван-дер - Ваальса. [34]
Легко видеть, что такая зависимость коэффициентов активности компонентов от состава получается как из уравнений Ван-Лаара, так и из уравнений Маргулеса при условии А В. [35]
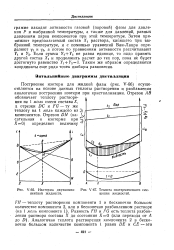 |
Изотерма двухкомпо - [ IMAGE ] - 67. Теплота изотермического сме. [36] |
Затем принимают предполагаемый состав Х раствора, кипящего при выбранной температуре, и с помощью уравнений Ван-Лаара определяют YI и Ya, а потом по уравнениям активности рассчитывают У. Таким же образом определяются координаты еще ряда точек изобары равновесия. [37]
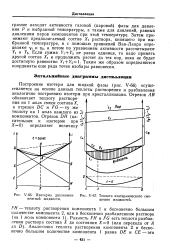 |
Изотерма двухкомпо - [ IMAGE ] - 67. Теплота изотермического сме. [38] |
Затем принимают предполагаемый состав Xi раствора, кипящего при выбранной температуре, и с помощью уравнений Ван-Лаара определяют YI и Y2, а потом по уравнениям активности рассчитывают YI и Yz. Таким же образом определяются координаты еще ряда точек изобары равновесия. [39]
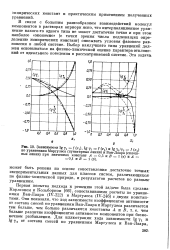 |
Зависимости lgflf ( xj, Ig Vz / ( i и Ig Vi / Vz / ( xj. [40] |
Первая попытка подхода к решению этой задачи была сделана Карлсоном и Кольборном [66], сопоставившими расчеты по уравнениям Ван-Лаара ( IV-222) и Маргулеса ( IV-246) с двумя константами. [41]
Уолом рассмотрен также случай, когда все три двойные системы, образующие тройную систему, могут быть описаны уравнениями Ван-Лаара. Однако мыслимы и нерассматривавшиеся в литературе промежуточные случаи, когда часть двойных систем описывается уравнениями Маргулеса, а часть - уравнениями Ван-Лаара. [42]
В этом расчете полагаем, что уг и у, зависят только от х ( как это следует из уравнения Ван-Лаара) и не зависят от температуры. [44]
Хотя в последнее время высказывались критические замечания по поводу точности уравнений Маргулеса [217], эти уравнения, как и уравнения Ван-Лаара, успешно использовались во многих работах. Музиль и Брейтенхубер [194] предложили уравнения с тремя константами, аналогичные уравнениям Маргулеса. Однако с технической точки зрения достигаемое при этом уточнение вряд ли компенсирует усложнение уравнений, обусловленное введением третьей константы. [45]
Страницы: 1 2 3 4
