Зарождение - радикал
Cтраница 1
 |
Спектры ЭПР перекисных радикалов при окислении. [1] |
Зарождение радикалов, как было установлено нами, осуществляется по тримолекулярной реакции [ см. схему, уравнение ( 0) ] v которая энергетически более выгодна, нежели ранее принятая ( по аналогии с газофазными процессами) бимолекулярная реакция. [2]
Зарождение радикалов происходит как на окислах, так и на металлических контактах. Подобная специфика этих процессов приводит к тому, что закономерности их протекания отличаются от закономерностей для истинно гетерогенных реакций. [3]
Зарождение радикалов ( реакция 1) и развитие цепи ( реакции 2 и 3) определяют только начальную стадию окисления полимеров, которая зависит от температуры, природы химических связей, образующих макромолекулы, наличия остатков катализаторов и структурного состава полимера. [4]
Зарождение радикалов ( реакция 1) и развитие цепи ( реакции 2 и 3) определяют только начальную стадию окисления полимеров, которая зависи от температуры, природы химических связей, образующих макромолекулы наличия остатков катализаторов и структурного состава полимера. [5]
Зарождение радикалов, как было установлено нами, осуществляется по тримолекулярной реакции [ см. схему, уравнение ( 0) ], которая энергетически более выгодна, нежели ранее принятая ( по аналогии с газофазными процессами) бимолекулярная реакция. [6]
Как оказалось, зарождение радикалов в ряде случаев осуществляется по тримолекулярной реакции 0, которая зачастую энергетически более выгодна, нежели ранее принятая ( по аналогии с газофазными процессами) бимолекулярная реакция. [7]
Для выяснения механизма зарождения радикалов на твердых поверхностях, по-видимому, также нужно исходить из химической точки зрения. Преобладающая роль химических факторов в процессе каталитического действия поверхности явствует из исключительной специфичности каталитических процессов. Рассматривая действие поверхности как результат химического взаимодействия активируемого вещества с катализатором, легко видеть, что рождение радикала на поверхности должно быть термодинамически более выгодным по сравнению с простой диссоциацией молекулы на радикалы. [8]
Для изучения процессов зарождения радикалов на поверхности гетерогенного катализатора в условиях жидкофазного окисления применен метод донорно-акцепторного и фотомодифицирования катализатора. [9]
Благодаря высокой скорости зарождения радикалов в водной фазе окисление углеводорода в гидроперекись происходит главным образом в этой фазе. На образование гидроперекиси в водной фазе указывает также ускоряющее действие водорастворимых солей кобальта и меди. [10]
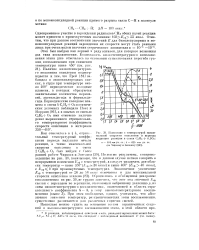 |
Изменение с температурой максимальной скорости окисления и периода индукции реакции в смеси С2Нв 0 502. а - 503 мм рт. ст.. б - 625 мм рт. ст. ( по Чиркову и Энтелису. [11] |
Одновременное участие в зарождении радикалов СН3 обоих путей реакции может привести к промежуточным значениям: 103 ф 55 ккал Отметим, что при данном соотношении значений Е для бимолекулярных и мономолекулярных реакций зарождения их скорости могут стать равными лишь при очень малом значении стерического множителя ы 10 - Ю 6 dTan был выбран как первый в ряду алкапов, для которого возможны два типа воспламенения. Наличие низкотемпературного механизма окисления подтверждается и тем, что Грей [81] наблюдал в этанокислородных смесях, в струе при температуре около 400 периодические холодные пламена, в которых образуются значительные количества перекисей, ацетальдегида и формальдегида. [12]
Механизм активации углеводородов и зарождения радикалов в процессах жидкофазного окисления до настоящего времени полностью не выяснен. [13]
Следует отметить, что зарождение радикалов путем термической диссоциации молекул может иметь существенное значение только при высоких температурах. Это является следствием высоких энергий связей, которые обычно подвергаются разрыву при таком типе зарождения. Лишь в том случае, когда в реакции участвуют сравнительно мало прочные соединения ( перекиси, азосоединения, нитриты и др.), подобное зарождение может происходить и при более низких температурах. [14]
Предположим, что реакция зарождения радикалов ( 0); является гетерогенной и протекает в условиях насыщенной адсорбции молекул алкана на стенках реактора. В этом случае, как известно, концентрация алкана в поверхностном слое, определяемая из уравнения адсорбционной изотермы для него, будет постоянной и скорость гетерогенного зарождения цепи будет также постоянной в достаточно большом интервале изменения давления или концентрации в газовой фазе. [15]
Страницы: 1 2 3 4