Металлирующий агент
Cтраница 2
Удивительным является тот факт, что пиперидид лития, который является более сильным металлирующим агентом, в то же время проявляет большую структурную избирательность, чем фениллитий. [16]
В процессе металлирования с помощью литийорганических соединений тиофена и его производных [13], атака происходит карбанионом металлирующего агента. [17]
Менее близко к литийорганическйм соединениям стоят соли некоторых тяжелых металлов, которые также нашли применение в качестве металлирующих агентов. Среди них наиболее известны соли двухвалентной ртути [132]; реакции замещения под действием этих солей исследовались еще в начальный период развития органической химии. Было найдено, что хлориды золота [133], теллура [134], таллия [135] и германия [136] также ме-таллируют некоторые ароматические ядра. Наличие в этих металлирующих агентах сильной кислоты Льюиса и отсутствие в них сильно основного аниона заставляет предполагать, что механизм их действия отличается от механизма действия металлоорганических соединений; только в случае меркурирования [137] механизм замещения водорода на атом тяжелого металла был исследован достаточно подробно. [18]
Калппоргаипческие соединения, получаемые in situ из литий-или натрийорганическнх соединений и алкоксидов калия, являются весьма активными металлирующими агентами [60]: они не только замещают аллильные или бензильные протоны, но и способны металлировать алксны [61] и циклопропаны. [19]
Действительно, как показал Виттиг, в реакции ( V - 4a) бутил-литий является более активным металлирующим агентом, чем метиллитий. [20]
Миллер и Диссельхоф [76] описали своеобразное металлирование по метиленовой группе диазометана при действии на последний трифенил -, метилнатрия как металлирующего агента. [21]
При взаимодействии ХПЭ с бутил - или фениллитием для увеличения выхода металлированного ПЭ в обратимой реакции замены хлора на литий целесообразно попользовать большой избыток металлирующего агента. Смещение равновесия в реакции RCl R Li RLi - f R Cl в желаемом направлении облегчается в присутствии сильно еольватмрующих растворителей, хотя последние и расщепляются IB известной степени литийорганическими соединениями. [22]
Реакции этого рода, аналогичные сопровождающимся перегруппировкой реакциям металлирования аммонийных солеи ( см. выше), протекают не только с литиевыми соединениями, но и с другими металлирующими агентами. [23]
Металлирующими агентами могут быть натриевые производные предельных углеводородов, амид натрия в жидком аммиаке и металлический натрий. Металли-рованию подвергаются преимущественно следующие группы органических соединений: ароматические углеводороды, жирноаро-матические соединения, ацетиленовые углеводороды. [24]
Однако можно предполагать, что поиски методов синтеза органических соединений кальция, бария и стронция будут продолжаться, так как каль-цийорганические соединения представляют несомненный интерес для целей препаративного синтеза. В некоторых случаях применение последних в качестве металлирующих агентов приводит к необычной ориентации заместителя ( см. стр. [25]
Однако можно предполагать, что поиски методов синтеза органических соединений кальция, бария и стронция будут продолжаться, так как каль-цийорган Ические соединения представляют несомненный интерес для целей препаративного синтеза. В некоторых случаях применение последних в качестве металлирующих агентов приводит к необычной ориентации заместителя ( см. стр. [26]
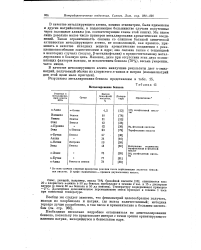 |
Металлирование бензола. [27] |
Мы знаем лишь довольно малое число примеров металлирования ароматических соединений. Такая ограниченность связана со слишком большой химической активностью металлирующего агента, не позволяющей, как правило, применять в качестве исходных веществ ароматические соединения с реак-ционноспособными заместителями в ядре; она связана также с тенденцией в некоторых случаях ( толуол, 3-метилнафталин) к предпочтительному метал-лированию в боковую цепь. Наконец, даже при отсутствии этих двух осложняющих факторов выходы, за исключением бензола ( 78 %), весьма умеренны, часто низки. [28]
Однако нитрильная, карбонильная и ряд других функциональных групп чувствительны к нуклеофильной атаке и поэтому могут присоединять RLi по кратной связи. Чтобы уменьшить вероятность такого процесса, нужно сделать так, чтобы металлирующий агент был сильно основным, но мало нуклеофильным, т.е. отщеплял протон быстрее, чем присоединялся к электронодефицитному атому углерода группы - CN или - COR. [29]
В результате дальнейших исследований стало очевидным, что в реакциях металлирования такого рода особенно эффективны лятийоргаиические соединения. Образование литийорганического соединения IV является типичным в отношении растворителя, экспериментальных условий и металлирующего агента. Типичной является также ориентация при металлировавии литийорганиче-скими соединениями. В таких реакциях вступающий атом металла обладает сильной тенденцией замещать тот атом водорода в ядре, который находится в орго-положении по отношению к гетероатому, или же атом водорода, находящийся в боковой цепи при атоме углерода, соседнем с гетероатомом. [30]
Страницы: 1 2 3 4