Проколлаген
Cтраница 1
Проколлагены, их химический состав, свойства и биологическая роль. [1]
 |
Кристаллический прокол-лаген. [2] |
Проколлаген, открытый В. Н. Ореховичем и А. А. Тустановским, по-видимому, является биологическим предшественником коллагена. Изучение свойств проколлагена показало, что он отличается от коллагена своим аминокислотным составом, а также тем, что расщепляется всеми ферментами, гидролизующими белки. [3]
Проколлагены, их химический состав, свойства и биологическая роль. [4]
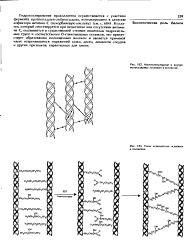 |
Межмолекулярные и внутримолекулярные сшивки в коллагене.| Типы ковалснтных сшивок в коллагене. [5] |
Гидроксилирование проколлагена осуществляется с участием фермеита протоколлаген-гидроксилазы, использующего в качестве кофактора аитамин С ( аскорбиновую кислоту) ( см. с. Коллаген, который синтезируется при недостатке или отсутствии витамина С, оказывается в существенной степени лишенным гидрокисль-ных групп и соответственно О-гликозильных остатков, что препятствует образованию полноценных волокон н является причиной часто встречающихся поражений кожи, десен, ломкости сосудов и других признаков, характерных для цинги. [6]
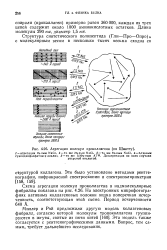 |
Агрегация молекул проколлагена ( по Шмитту. [7] |
Схема агрегации молекул проколлагена в надмолекулярные фибриллы показана на рис. 4.26. На электронных микрофотографиях нативных коллагеновых волокон видна поперечная исчер-ченность, соответствующая этой схеме. [8]
Протелин, подобно проназе, расщепляет проколлаген из шкуры теленка. Действие протелина на проколлаген значительно глубже действия трипсина. При отношении фермент: субстрат 1: 10, температуре 30 и продолжительности протеолиза 24 часа протелин расщепляет в монрмере коллагена ( молекулярный вес 260000) 21 пептидную связь, в то время как трипсин гидролизует только три связи. [9]
При умеренном нагревании и растворах молекулы проколлагена распадаются па а - н р-комноненты. [10]
Образование тройной спнралн в центре молекулы проколлагена. [11]
Полученные двухмерные бумажные хроматограммы дали возможность установить, что проколлагены, выделенные из кожи человека и позвоночных животных, содержат следующие аминокислоты: аспарагиновую кислоту, глютаминовую кислоту, серии, гликокол, лизин, аргинин, аланин, гистидин, оксипролин, пролин, валин, лейцин, фенилаланин. По составу аминокислот, проявляющихся на хроматограммах, проколлагены оказались близкими к желатине, отличаясь от нее отсутствием тирозина. [12]
Коллагеновые волокна ( фибриллы) образуются при агрегации цепей проколлагена. Эти фибриллы играют роль центров кристаллизации при остеогенезе, росте костей. [13]
Коллагеновые волокна ( фибриллы) образуются при агрегации цепей проколлагена. [14]
В С-концевых пропептидах локализованы межцепьевые связи 3 - 3, стабилизирующие молекулы проколлагена. [15]
Страницы: 1 2 3 4