Проколлаген
Cтраница 3
 |
Схема биосинтеза коллагена. [31] |
Биосинтез коллагена, осуществляемый в фибробластах, протекает весьма сложно. Сначала его цепи синтезируются иа полисомах в виде предшественников, образуя проколлаген. В частности, предшественники al - и a2 - цепей имеют молекулярную массу свыше 120 000 каждый. [32]
Коллаген, как все фибриллярные белки, почти нерастворим в нейтраль ных растворах солей, слабых кислотах и щелочах. Коллаген, экстрагируемый цитратным буфером рН 4 0 из кожи различных животных, назван проколлагеном и наряду с тропоколлагеном, который экстрагируют нейтральными растворами солей, используется при исследовании физических и химических свойств коллагеновой молекулы. [33]
Кожа представляет собой сложное переплетение коллагеновых волокон. Структуру коллагеновой фибриллы в целом можно представить как продольно расположенные нити колластромина диаметром около 100 А, вокруг которых размещены различные образования проколлагена [ 136, 137, с. Следовательно, коллагеновая фибрилла - гетерогенная система, состоящая по крайней мере из двух фаз. [34]
 |
Термодинамические характеристики денатурации тропоколлагена. [35] |
При осторожном нагревании коллагена с водой при 62 - 63 С волокна испытывают необратимое сокращение примерно в три раза. По-видимому, этот переход, являющийся кон-формационным превращением, обусловлен кооперативным разрушением водородных и гидрофобных связей. Проколлаген испытывает тепловой переход и в растворе. [36]
Его отличие от коллагена заключается в продлении jV - концевого сегмента, содержащего дисульфидные связи и триптофан. Превращение проколлагена в коллаген осуществляется вне клетки ферментом проколлагенпептидазой, удаляющей содержащий цистин и триптофан jV - концевой сегмент посредством расщепления связи X-Glu или X-Gln, в результате чего на N-конце коллагена образуется остаток пирролидон-2 - карбо-новой-5 кислоты. Об этой протеазе известно мало, за исключением того, что она содержит важный для активности металл и не является ни сериновой, ни тиольной протеиназой. Наследственное заболевание крупного рогатого скота, дерматоспараксис, объясняется отсутствием этой протеолитической стадии. Коллаген состоит из трех полипептидных цепей, в каждой из которых содержится около 1000 аминокислотных остатков. У N - и С-концов коллагена расположены неспиральные телопеп-тидные участки. [37]
По своему аминокислотному составу проколлагены отличаются от коллагена главным образом содержанием тирозина, фенилаланина, гистидина, пролина и оксипролина. Содержание фенилаланина в проколлагенах приблизительно вдвое меньше, чем в коллагене, содержание же гистидина в проколлагенах, наоборот, значительно выше. Проколлагены нерастворимы в чистой воде и сравнительно слабо растворимы в подкисленной воде и в кислых буферных растворах с невысокой концентрацией солей. [38]
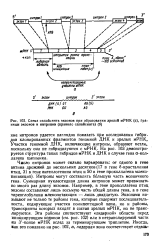 |
Схема сплайсинга экзонов при образовании зрелой мРНК ( а, границы экзоиов и нитронов ( правило сплайсинга ( б. [39] |
Интроны могут составлять большую часть мозаичного гена. Суммарная нуклеотидная длина нитронов может превышать во много раз длину экзонов. Например, в гене проколлагена птиц экзоны составляют лишь восьмую часть общей длины гена, а в гене тиреоглобулина млекопитающих - лишь двадцатую. Экзонами называют не только те районы гена, которые содержат последовательности, кодирующие участки полипептидной цепи, но и районы, транскрипты которых входят в состав зрелых мРНК, но не транслируются. Эти районы соответствуют лидерной области перед инициирующим кодовом ( см. рис. 102) или в нетранслируемой части на 3 -конце мРНК вслед за терминирующим триплетом. [40]
 |
Схема сплайсинга экзонов при образовании зрелой мРНК ( а, границы экзоиов и нитронов ( правило сплайсинга ( б. [41] |
Интроны могут составлять большую часть мозаичного гена. Суммарная нуклеотидная длина интронов может превышать во много раз длину экзонов. Например, в гене проколлагена птиц экзоны составляют лишь восьмую часть общей длины гена, а в гене тиреоглобулина млекопитающих - лишь двадцатую. Экзонами называют не только те районы гена, которые содержат последовательности, кодирующие участки полипептидной цепи, но и районы, транскрипты которых входят в состав зрелых мРНК, но не транслируются. Эти районы соответствуют лидерной области перед инициирующим кодоном ( см. рис. 102) или в нетранслируемой части на 3 -конце мРНК вслед за терминирующим триплетом. [42]
Отличительной чертой остеобластов является наличие сильно развитого эндоплазматического ретикулума и мощного аппарата белкового синтеза. В результате действия группы специальных пептидаз от проколлагена отщепляются сначала N-концевой, а затем С-концевой домены и формируется тропо-коллаген. Последний в межклеточном пространстве образует фибриллы. В дальнейшем после образования поперечных сшивок формируется зрелый коллаген ( см. гл. [43]
Фибробласты, которые синтезируют коллаген, секретируют также фибронектин - гликопротеин, присутствующий на поверхности клеток, в межклеточном веществе и крови. Фибронектин связывается с агрегирующими проколлагеновыми волокнами и оказывает влияние на формирование околоклеточного матрикса. В межклеточном веществе происходит ассоциация фибронектина, проколлагена с протеогликанами, гепаринсульфатами и хондроитинсульфатами. Так, например, IX тип коллагена ( из хрящей) содержит протеоглика-новые цепи. [44]
При экстрагировании соединительной гкани холодными растворами солей, разбавленными уксусной кислотой ( рНЗ 9), а также растворами щелочей часть коллагена переходит в раствор. Эти растворяющиеся молекулы при любом способе экстракции практически идентичны. Часть коллагена, растворимую в кислоте, принято называть проколлагеном. [45]
Страницы: 1 2 3 4