Протекание - электрохимическая реакция
Cтраница 1
Протекание электрохимических реакций (6.1) и (6.21) в одну элементарную стадию является маловероятным. Если исходить из принципа Франка - Кондона ( см. гл. [1]
Протекание электрохимической реакции приводит к тому, что не все количество электричества расходуется на заряжение двойного слоя, а часть его проходит через границу раздела электрод - электролит. Здесь в качестве электрохимического аналога следует взять цепь, состоящую из емкости и параллельно включенного сопротивления. Емкость конденсатора отвечает при этом емкости двойного электрического слоя, а сопротивление ( при известных условиях) можно рассматривать как величину, обратную скорости протекания электрохимической реакции. Изучение зависимости емкости двойного слоя и его электрического сопротивления от потенциала с помощью соответствующих схем на переменном токе является еще одним эффективным методом исследования кинетики электрохимических реакций. Данные о емкости двойного слоя позволяют судить о состоянии поверхности электрода и о характере адсорбции на электроде различных веществ. [2]
Поскольку протекание электрохимической реакции связано с поляризацией электрода, то в кулонометрии потенциал рабочего электрода, так же как в вольтамперометрии, значительно отличается от его равновесного значения. [3]
 |
Потенциал нулевого заряда. [4] |
Для протекания электрохимических реакций большое значение имеет величина падения потенциала в диффузной части двойного слоя. Обычно эту величину обозначают через ф и называют пси-прим-потенииа. [5]
 |
Схема химического источника тока ( в и электролитической ванны ( б. [6] |
Для протекания электрохимической реакции это условие является необходимым. [7]
Скорость протекания электрохимической реакции в анодную и катодную стороны одинакова на равновесном электроде как в целом, так и на любом его участке, достаточно большом по сравнению с размерами молекул. [8]
Скорость протекания электрохимической реакции в анодную и катодную стороны одинакова на равновесном электроде в целом и на любом его участке, достаточно большом по сравнению с размерами молекул. [9]
Скорость протекания электрохимической реакции в анодную и катодную стороны одинакова на равновесном электроде как в целом, так и на любом его участке, достаточно большом по сравнению с размерами молекул. [10]
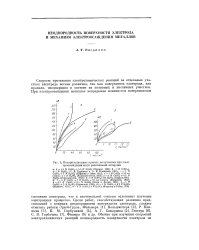 |
Поляризационные кривые, полученные при электроосаждении модн различными авторами. [11] |
Скорость протекания электрохимических реакций па отдельных участках электрода весьма различна, так как поверхность электрода, как правило, неоднородна и состоит из активных и пассивных участков. [12]
При протекании электрохимической реакции концентрация участников реакции в приэлектродном слое изменяется - возрастает или убывает - по сравнению с концентрацией в глубине раствора. [13]
При протекании электрохимической реакции могут адсорбироваться деполяризатор, продукт реакции или неэлектроактивные вещества, находящиеся в исследуемом растворе. [14]
 |
Схема строения диффузного двойного электрического слоя. [15] |
Страницы: 1 2 3 4