Протекание - электрохимическая реакция
Cтраница 2
При протекании электрохимических реакций на границе между электродом и раствором возникает двойной электрический слой. Он образуется за счет электрических зарядов, находящихся на электроде, и ионов противоположного знака ( противоионов), ориентированных в растворе у поверхности электрода. Благодаря этому создается скачок потенциала на границе электрод-раствор. [16]
При протекании электрохимической реакции концентрация участников реакции в приэлектродном слое изменяется - возрастает или убывает - по сравнению с концентрацией в глубине раствора. [17]
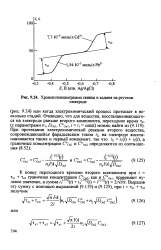 |
Хронопотенциограмма свинца и кадмия на ртутном. [18] |
При протекании электрохимической реакции второго вещества, сопровождающейся фарадеевским током / 2, на электроде восстанавливается также и первый компонент, так что h i ( t) h ( t a граничные концентрации C oxi и С оа. [19]
При протекании электрохимической реакции восстановления анионов малеиновой кислоты образуются ионы гидроксила [83], ускоряющие протекание обратной реакции ( I), приводящей к исчезновению электрохимически активной формы деполяризатора, поэтому толщина реакционного слоя ц, является функцией протекающего тока [82, 83]: чем выше ток, тем тоньше реакционный слой. Величина же б не зависит от силы тока, следовательно, отношение u / б падает по мере увеличения тока на подъеме волны. С ростом концентрации КС1 волна становится положительное, причем в верхней части волны, где, как уже указывалось, отдошение u / б меньше, скорость протонизации повышается сильнее, чем в нижней, что приводит к большему относительному увеличению тока в верхней части волны. Этот эффект обусловливает увеличение крутизны волны и больший сдвиг к положительным потенциалам ее верхней части, чем нижней. [20]
Как и протекание других электрохимических реакций, процесс выделения металла на ртути и амальгаме является стадийным. В общем случае при электроосаждении могут происходить: диффузия реагирующей частицы к электроду, ее химическое превращение в объеме раствора или у поверхности электрода с последующей адсорбцией, первичная адсорбция с последующей гетерогенной химической реакцией, частичная десольватация или потеря лигандов, разряд и диффузия атома вглубь жидкой фазы электрода. Отдельные стадии этого сложного процесса, за исключением стадии диффузии и разряда, могут отсутствовать. При исследовании осаждения металлов экспериментально удается выделить стадии диффузии, химической реакции, адсорбции и разряда. [21]
Реальная возможность протекания электрохимических реакций в режиме безбарьерного разряда определяется наличием дополнительного фактора. Дело в том, что безактивационный разряд протекает без затруднений, поэтому все ионы, которые разряжаются на электроде в безбарьерном режиме, должны сразу же ионизироваться и результирующая плотность катодного тока неизбежно будет равна нулю. Но если имеется достаточно быстрая стадия удаления продукта электрохимической реакции ( например, в рассматриваемом случае - безактивационная электрохимическая десорбция), то восстановившиеся частицы не успевают вновь окислиться. Вследствие этого восстановление ионов становится возможным. [22]
Для уменьшения протекания электрохимических реакций окисления, рекомендуется обертывать аноды толстой, но рыхлой тканью типа фильтровального сукна. [23]
Сд и на протекание электрохимической реакции, имеющей комплексное псевдосопротивление Zcj; эти составляющие соединены параллельно. [24]
Скорость и механизм протекания электрохимических реакций изучает электрохимическая кинетика, или кинетика электродных процессов. Особенностью электрохимических реакций служит влияние потенциала на их скорость. Любая электрохимическая реакция протекает минимум в три стадии: а) подвод реагентов к электроду; б) собственно электрохимическая реакция, которая может включать в себя и химические реакции; в) отвод продуктов реакции от электрода. Если бы все эти стадии протекали мгновенно, то потенциал электрода при прохождении тока не изменялся бы и соответственно поляризация была бы равна нулю. Следовательно, возникновение поляризации обусловлено замед-ленностью отдельных стадий электрохимического процесса. Соответственно в зависимости от характера замедленной стадии на электроде возникает или концентрационная, или электрохимическая поляризация. [25]
Скорость и механизм протекания электрохимических реакций изучает электрохимическая кинетика, или кинетика электродных процессов. Особенностью электрохимических реакций служит влияние потенциала vil. Поляриза - на их скорость. [26]
С точки зрения протекания различных электрохимических реакций важны перенапряжения водорода на катоде и кислорода на аноде, от кторых зависят максимальные электродные потенциалы катода и анода, возможные для данного материала электродов в данной среде и при данной температуре. При максимальных - потенциалах на катоде начинается выделение водорода, а на аноде - кислорода, и весь избыток электрической энергии, подаваемой на электроды, расходуется на электролиз воды. [27]
Ток, обусловленный протеканием электрохимической реакции. Если при проведении хронопотенциометрических исследований задать достаточно большую силу тока, то потенциал электрода достигает такого значения, при котором начинается разложение фона: на отрицательной стороне - восстановление катионов, а на положительной-растворение ртути электрода, связанное с образованием соединений ртути с анионами. В этом случае потенциал электрода остается постоянным, а подводимые к его поверхности заряды расходуются на электрохимическую реакцию. Как только направление тока изменяется, меняется заряд электрода и его потенциал приобретает другое крайнее значение, при котором начинает протекать противоположная электрохимическая реакция с участием других ионов фона. [28]
Вопросы, связанные с протеканием электрохимических реакций в жидких кристаллах [7, 26], выходят за рамки данной книги. Мы рассмотрим здесь лишь некоторые физические следствия приэлектродных процессов. [29]
Вследствие расхода деполяризатора при протекании электрохимической реакции его концентрация становится минимальной непосредственно у электродной поверхности и по мере удаления от электрода концентрация деполяризатора постепенно увеличивается, приближаясь к ее величине в глубине раствора. С увеличением времени электролиза концентрация деполяризатора падает как у поверхности электрода, так и в прилегающем к ней объеме раствора, при этом с увеличением продолжительности электролиза область раствора, обедненного деполяризатором, постепенно расширяется. [30]
Страницы: 1 2 3 4