Протекание - электрохимическая реакция
Cтраница 3
Таким образом, при протекании электрохимических реакций потребляются или освобождаются4 электроны. Оба типа реакций могут протекать пространственно раздельно или на общей поверхности. Если реакции пространственно отделены друг от друга, то освобождающиеся в результате окисления электроны поступают в зону восстановления через внешнюю цепь. [31]
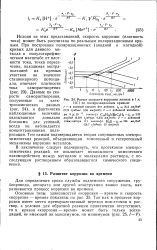
Различие между двумя способами контропя протекания электрохимической реакции показано на рис. 5.1 Кривая / схематически изображает связь между током, протекающим через ячейку, и потенциалом рабочего электрода Исходный раствор содержит два восставав пивающихся соединения или одно соединение с двумя группами, восстанавливающимися при различных потенциалах. [32]
 |
Расчет скорости коррозии железа в 1 к. [33] |
В заключение следует подчеркнуть, что протекание электрохимических реакций не исключает возможности химического взаимодействия между металлом и молекулами раствора, с последующим растворением образовавшегося химического соединения. [34]
В растворах для химической металлизации возможно протекание электрохимической реакции окисления восстановителя и восстановления ионов металла в объеме раствора. [35]
Выше мы предполагали, что при протекании электрохимической реакции лимитирующей является либо стадия массопереноса, либо стадия разряда - ионизации. В реальных условиях кинетика электродных процессов всегда в той или иной степени зависит от скорости обеих этих стадий. В связи с этим рассмотрим протекание электрохимической реакции ( А) в условиях смешанной кинетики, когда 1Ф определяется одновременно и скоростью массопереноса веществ Ох и Red, и скоростью перехода электронов через границу электрод / раствор. [36]
Таким образом, несмотря на принципиальную возможность протекания электрохимических реакций по термоэмиссионному механизму, вклад этого механизма в регистрируемый ток для исследованных в водных растворах процессов оказывается ничтожно малым по сравнению с вкладом, который обеспечивается механизмом разряда-ионизации. [37]
Покажем теперь, что для рассматриваемого конкретного механизма протекания электрохимической реакции такие важные параметры электродного импеданса, как эффективные числа электронов кх и nz, переносимых на отдельных адсорбционных стадиях, а также производная от электрохимического потенциала вещества в адсорбционном состоянии по адсорбированному количеству РА могут быть определены независимым от импедансных измерений путем, а именно на основе термодинамических адсорбционных данных для обратимого электрода. [38]
Характеристика топливного элемента такого типа определяется как скоростью протекания электрохимических реакций на электродах, так и скоростью химических реакций регенерации промежуточных веществ. В качестве промежуточных окислителей и восстановителей применяются, как правило, неорганические ибны, скорость электрохимических превращений которых велика; поэтому сама электрохимическая реакция обычно не лимитирует общей скорости реакции. Некоторые потери в самом топливном элементе возникают в сопротивлении диафрагмы. Последняя находится под воздействием как окисляющих, так и восстанавливающих растворов и должна обладать достаточной толщиной, чтобы не подвергаться быстрому разрушению. Электрическое сопротивление диафрагмы в значительной степени обусловливает снижение напряжения элемента при росте плотности тока. [39]
 |
Схема моста, применяемого для измерения импеданса ( комплексного сопротивления межфазной границы электрод-электролит. [40] |
Однако при измерениях не удается полностью исключить возможность протекания электрохимических реакций на поверхности электрода. [41]
 |
Уравновешивание электродвижущей силы гальванической цепи разностью потенциалов, подаваемой от потенциометрической схемы. [42] |
В рассматриваемом здесь случае направление течения электронов соответствует протеканию электрохимической реакции слева направо. Таким образом, степень превращения возрастает, и величина dg положительна. [43]
Спс - так называемая псевдоемкость, связанная с протеканием электрохимической реакции. Адсорбция заряженных частиц по-разному влияет на оба этих слагаемых, а изменение емкости влечет за собой изменение емкостного тока и формы полярограммы. [44]
Гальваностатический метод изучения процесса также позволяет установить степень затруднения протекания электрохимических реакций при изменении рН в растворах фиолетовой и зеленой модификаций. При этом найдена линейная зависимость между потенциалом восстановления и величиной рН раствора при заданной плотности тока. [45]
Страницы: 1 2 3 4