Протон - метиленовая группа
Cтраница 3
В случае соединений, содержащих двукратно активированную метиленовую группу, реакция чаще всего сопровождается дегидратацией ( вследствие большой подвижности обоих протонов метиленовой группы. [31]
При рассмотрении этого механизма перегруппировки можно заметить, что с экспериментальным фактом отсутствия в продуктах реакции енонов хорошо согласуется положение о большой подвижности протона метиленовой группы, которое следует из рассмотрения строения ( - ацетиленового спирта. [32]
Для раци-изомера ( V) встречается кон-формер, имеющий о сь С2, относительно которой взаимозаменяются как протоны при С2 я С4, так и протоны метиленовой группы. Поэтому протоны каждой пары химически эквивалентны. [33]
Стрелки под метиленовой группой изображают ориентации ( относительно направления поля Но), которые могут принимать спины протонов метильной группы; стрелки под метильной группой показывают возможные ориентации спинов протонов метиленовой группы. [35]
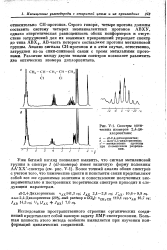 |
Спектры оптических изомеров 2 4-дихлорпентана. [36] |
Строго говоря, четыре протона должны составить систему четырех неэквивалентных протонов АВХУ, однако энергетическая равноценность обоих конформеров и отсутствие затруднений для их взаимных превращений упрощает спектр до типа АВХ2, АВ-часть которого составляют протоны метиленовой группы. Анализ сигнала СН-протонов и в этом случае, естественно, затруднен из-за спин-спиновой связи с тремя метальными протонами. Различие между двумя типами спектров позволяет различить два оптических изомера дихлорпентана. [37]
Рассмотрим пример применения ЯМР для решения такой задачи путем изучения ФС катализатов крекинга, полученных на свежем, отравленном и реактивированном образцах промышленного микросферического цеолитсодержащего катализатора [438, 439] Характеристики ФС таких катализатов, элементный состав и содержание в них бензина представлены в табл 3 49 В результате реактивации катализатора количество а-протонов по отношению к ароматическим ядрам и протонов метиленовых групп в алкильных цепях снижается и приближается к уровню в катализате на неотравленном катализаторе, хотя количество протонов концевых групп алкильных цепей для всех катализатов одинаково В катализате, полученном на реактивированном катализаторе, зафиксировано наибольшее содержание ароматических и наименьшее содержание бензильных протонов, что связано со снижением степени замещения ароматических колец ( т е после пассивации в катализате преобладают алкилбензолы с невысокой степенью замещения колец) Параметр ароматичности изменяется незначительно Содержание третичных и четвертичных углеродных атомов после пассивации превосходит таковое для катализатов, полученных как на отравленном, так и на свежем катализаторе. [38]
В свою очередь протоны соседних метиленовых групп могут дать квартет, если их КССВ с протоном ОН-группы и протонами метиленовой группы одинакова, или дублет триплетов, если эти константы не равны. Кроме того, в теоретическом спектре ПМР-13 - пропандиола должен присутствовать мультиплет метиленовой группы, не связанной непосредственно с атомами кислорода. Таким образом, в теоретическом спектре рассматриваемого двухатомного спирта должны быть три мультипле-та протонов трех неэквивалентных групп, в то время как в спектре ПМР, приведенном в задаче, есть всего лишь сигналы от двух неэквивалентных групп протонов. Следовательно, этот спектр не отвечает ни диэтиловому эфиру, ни 1 3-пропандиолу. [39]
Наконец, заместители такого типа мало влияют ( или совсем не влияют) на реакции анионов нечетных альтернантных углеводородов. Так, например, протоны метиленовой группы в а-мет-оксиацетофеноне CeHsCOCHoCOCHs мало отличаются по кислотности от протонов метильной группы в ацетофеноне. [40]
Из приведенных данных видно, что амид этиленгликольфосфористой кислоты имеет сигнал метиленовых протонов в наиболее сильном поле по сравнению с другими производными. Это свидетельствует о большем экранировании протонов метиленовых групп кольца. [41]
В молекулах, где спины протонов метиленовой группы ориентированы в противоположные стороны ( оф и ра), протоны метильной группы не будут испытывать их влияния ввиду взаимной компенсации дополнительных полей, создаваемых двумя протонами. В молекулах, где спины обоих протонов метиленовой группы направлены по полю ( аа) или против него ( РР), протоны метильной группы будут испытывать влияние дополнительного поля и их резонанс будет смещен в более сильное или более слабое поле по сравнению с предыдущим случаем. [42]
 |
Возможные ориентации спинов протонов СН2 - группы ( - направление проекции спина вдоль направления Н0. [ - против направления Н0. [43] |
В молекулах, где спины протонов метиленовой группы ориентированы в противоположные стороны ( ар и Ра), протоны метильной группы не будут испытывать их влияния ввиду взаимной компенсации дополнительных полей, создаваемых двумя протонами. В молекулах, где спины обоих протонов метиленовой группы направлены по полю ( аа) или против него ( РР), протоны метильной группы будут испытывать влияние дополнительного поля и их резонанс будет смещен в более сильное или более слабое поле по сравнению с предыдущим случаем. [44]
Расщепление на протоне при центральном атоме углерода в аллильном радикале равно 4 06 Гс, на концевых протонах составляет 13 93 и 14 83 Гс. Приняв среднее значение для расщепления на протонах метиленовых групп, рассчитайте е в уравнении ( 6 - 16) из отношения констант сверхтонкого расщепления. [45]
Страницы: 1 2 3 4
