Процесс - электрохимическая коррозия
Cтраница 2
Процесс электрохимической коррозии в почве значительно сложнее, чем в атмосфере или в воде, главным образом потому, что почвы задерживают различное количество влаги в капиллярах и порах. Например, песчаные почвы гораздо менее агрессивны, чем глинистые. [16]
Процессы электрохимической коррозии могут развиваться не только в больших объемах электролитов, но и в тонких пленках влаги, конденсирующейся на поверхности изделия. Типичным примером электрохимической коррозии в тонкой пленке является атмосферная коррозия. [17]
Процесс электрохимической коррозии развивается на границе раздела двух фаз - металла и раствора электролита, где образуются два слоя: в металле у поверхности атомы ионизированы - и в растворе против металлических ионов располагаются ионы из электролита с противоположным зарядом. Возникновение таких слоев приводит к образованию разности потенциалов. [18]
Процессы электрохимической коррозии могут развиваться не только в больших объемах электролитов, но и в тонких пленках влаги, конденсирующейся на поверхности изделия. Типичным примером электрохимической коррозии в тонкой пленке является атмосферная коррозия. [19]
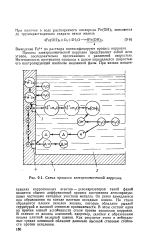 |
Схема процесса электрохимической коррозии. [20] |
Процесс электрохимической коррозии представляет собой цепь этапов, последовательно протекающих с различной скоростью. Интенсивность протекания процесса в целом определяется скоростью его контролирующей наиболее медленной фазы. [21]
Процессы электрохимической коррозии протекают следующим образом. [22]
Процессы электрохимической коррозии протекают в водных растворах. При соприкосновении металлической поверхности с раствором электролита происходит взаимодействие металла с заряженными частицами раствора и переход ионов метала в раствор. [23]
Процесс электрохимической коррозии представляет собой совокупность двух сопряженно протекающих реакций. [24]
 |
Потери массы при коррозии и гидроэрозии различных материалов. [25] |
Процесс электрохимической коррозии является одним из факторов, постоянно сопутствующих гидроэрозии металлов. [26]
Процессы электрохимической коррозии описываются законами электрохимической кинетики. При этом процессе протекают две группы реакции: катодная и анодная. За счет возникающего электрического тока может иметь место удаление продуктов коррозии от очагов разрушения. На скорость процесса коррозии существенное влияние оказывает технология изготовления конструктивного элемента аппарата. [27]
Этот процесс электрохимической коррозии через некоторое время замедляется в результате уменьшения создаваемой микроэлектродами электродвижущей силы, происходящего вследствие, во-первых, различной скорости протекаемых на электродах процессов и, во-вторых, вследствие незначительной скорости диффундирования в глубину раствора перешедших в воду ионов металла. Это снижение силы тока называется поляризацией. [28]
Возможны процессы электрохимической коррозии. [29]
 |
Примеры разъедания поверхностей. [30] |
Страницы: 1 2 3 4