Процесс - катодное выделение - водород
Cтраница 1
Процесс катодного выделения водорода на ртути и подобных катодах происходит по механизму замедленный разряд - электрохимическая десорбция. Естественно, что суммарная скорость перехода какого-либо изотопа из раствора в газ определяется не только скоростью его разряда, но и скоростью его электрохимической десорбции. [1]
 |
Средние коэффициенты активности хлористых натрия и калия в водных растворах. [2] |
С измеримой скоростью процесс катодного выделения водорода по приведенной выше реакции вблизи равновесного потенциала может идти только на платинированной платине в условиях идеальной чистоты раствора. Практически выделение водорода происходит с перенапряжением. [3]
Фрумкиньш применительно к процессу катодного выделения водорода. Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно - активных, способных изменить величину - потенциала. [4]
Фрумкиным применительно к процессу катодного выделения водорода Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно-активных, способных изменить величину - потенциала. В частном случае ( яр. [5]
Фрумкиным применительно к процессу катодного выделения водорода. Из формулы Фрумкина вытекает, что перенапряжение зависит не только от концентрации непосредственных участников электродной реакции, но и от природы и содержания любых веществ, в первую очередь поверхностно-активных, способных изменить величину я - потенциала. В частном случае ( i 0) она превращается в формулу Эрдей-Груза и Фоль-мера. [6]
Тафелем, который рассматривал процесс катодного выделения водорода и предполагал, что медленной стадией этого процесса является рекомбинация атомов водорода в молекулу водорода. Поэтому теорию выделения водорода, предложенную Тафелем, называют рекомбинационной теорией. Так как для выделения водорода по механизму Тафеля р2 и м1, то наклон поляризационной кривой в координатах TI - lg i при больших ц должен быть равным 2 З Г / 2 / - 29 мВ при 25 С. Рекомбинационная теория не позволяет ( без дополнительных предположений) также объяснить зависимость TI от рИ и состава раствора и оказывается, таким образом, неприменимой к процессу катодного выделения водорода на ртути. [7]
Тафелем, который рассматривал процесс катодного выделения водорода и предполагал, что медленной стадией этого процесса является рекомбинация атомов водорода в молекулу водорода. Поэтому теорию выделения водорода, предложенную Тафелем называют рекомбинацион-ной теорией. Так как для выделения водорода по механизму Та-феля р2 и л1, то наклон поляризационной кривой в координатах ц - Igi при больших т ] должен быть равным 2 3 RT / 2F - - 29 мВ при 25 С. Реком-бинационная теория не позволяет ( без дополнительных предположений) также объяснить зависимость т ] от рН и состава раствора и оказывается, таким образом, неприменимой к процессу катодного выделения водорода на ртути. [8]
Заключение об истинной природе процесса катодного выделения водорода может быть сделано на основании сопоставления закономерностей, вытекающих из данного кинетического механизма, с опытным материалом. Наиболее важные из этих закономерностей можно рассматривать как критерии справедливости той или иной теории водородного перенапряжения. [9]
Теория электрохимического перенапряжения была разработана применительно к процессу катодного выделения водорода, а затем распространена на другие электродные процессы. Основой этой теории служит классическое учение о кинетике гетерогенных химических реакций. Количественные соотношения между величиной перенапряжения ц и плотностью тока / были получены при использовании принципа Бренстеда о параллелизме между энергией активации Ua и тепловым эффектом QP ( или изобарным потенциалом AG) в ряду аналогичных реакций. Квантовомеханическая трактовка электродных процессов начала формироваться лишь сравнительно недавно, хотя отдельные попытки в этом направлении предпринимались уже начиная с середины 30 - х годов ( Герни, О. А. Есин и Др. [10]
Теория электрохимического перенапряжения была разработана применительно к процессу катодного выделения водорода, а затем распространена на другие электродные процессы. Основой этой теории служит классическое учение о кинетике гетерогенных химических реакций. Количественные соотношения между величиной перенапряжения ц и плотностью тока i были получены при использовании принципа Бренстеда о параллелизме между энергией активации t / а и тепловым эффектом Qp ( или изобарным потенциалом AG) в ряду аналогичных, реакций. Основные исследования, в этом направлении были выполнены Христовым, Маркусом, Левйчем и рядом других авторов. Изложение работ по квантовомеханической теории электродных процессов выходит за рамки настоящего курса. [11]
Теория электрохимического перенапряжения была разработана применительно к процессу катодного выделения водорода, а затем распространена на другие электродные процессы. Основой этой теории служит классическое учение о кинетике гетерогенных химических реакций. Количественные соотношения между величиной перенапряжения т ] и плотностью тока / были получены при использовании принципа Бренстеда о параллелизме между энергией активации Ua и тепловым эффектом QP ( или изобарным потенциалом AG) в ряду аналогичных реакций. [12]
На основе применения мультиплетной теории Баландина к процессам катодного выделения водорода на различных металлах выведено уравнение, выражающее зависимость перенапряжения водорода от атомного радиуса металла. Полученное уравнение для многих металлов описывает опытнонаблюдаемую зависимость константы уравнения Тафеля от атомных радиусов металла. [13]
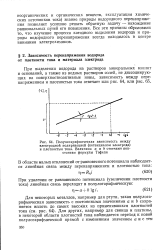 |
Полулогарифмическая зависимость между. [14] |
Все эти причины обусловили то, что изучение процесса катодного выделения водорода и природы водородного перенапряжения всегда находилось в центре внимания электрохимиков. [15]
Страницы: 1 2 3 4