Процесс - катодное выделение - водород
Cтраница 3
Величина перенапряжения водорода и характер ее зависимости от различных факторов должны находиться поэтому в тесной связи с природой процесса катодного выделения водорода. Изучение водородного перенапряжения позволяет выяснить механизм этой реакции и представляет большой интерес с теоретической точки зрения. Закономерности, установленные при изучении перенапряжения водорода, можно частично распространить и на другие случаи электрохимической кинетики. Это еще более повышает теоретическую значимость работ по водородному перенапряжению. Изучение водородного перенапряжения имеет также большое практическое значение. Величина водородного перенапряжения составляет значительную долю напряжения на ваннах по электролизу воды и растворов хлоридов. Знание природы водородного перенапряжения позволяет его уменьшать, а следовательно, и снижать расход электроэнергии и улучшать экономические показатели этих процессов. [31]
Величина перенапряжения водорода и характер ее зависимости от различных факторов должны находиться поэтому в тесной связи с природой процесса катодного выделения водорода. [32]
Необходимость в прижимных стальных планках вызвана тем, что не закрепленная механически гуммировка постепенно отрывается и вздувается в процессе катодного выделения водорода, постепенно распространяющегося под слой гуммировки. [33]
Многочисленные исследования, проведенные после Та-феля, подтвердили справедливость уравнения (3.21) в весьма широком интервале плотностей тока как для процесса катодного выделения водорода, так и для большого количества других как катодных, так и анодных процессов. [34]
Интересно отметить следующее: ДСК-электрод, состоящий из тела-носителя из одного карбонильного никеля и напеченного на него слоя сплава Ренея толщиной, равной лишь диаметру зерен, в процессе катодного выделения водорода вел себя, как чистый носитель без этого слоя. Отсюда, со всей очевидностью следует, что при уменьшении толщины слоя активного материала в конце концов все же наступает ухудшение характеристики процесса выделения. [35]
Интересно отметить следующее: ДСК-электрод, состоящий из тела-носителя из одного карбонильного никеля и напеченного на него слоя сплава Ренея толщиной, равной лишь диаметру зерен, в процессе катодного выделения водорода вел себя как чистый носитель без этого слоя. Отсюда со всей очевидностью следует, что при уменьшении толщины слоя активного материала в конце концов все же наступает ухудшение характеристики процесса выделения. [36]
Такой случай реализуется при выделении водорода на ртутном катоде из водных растворов угольной кислоты. Слабые органические основания способны катализировать процесс катодного выделения водорода. [37]
Рекомбинационная теория без дополнительных предположений не позволяет также объяснить зависимость перенапряжения от рН и состава раствора. Поэтому рекомбинационная теория неприменима к процессу катодного выделения водорода на ртутном электроде. [38]
Практически ни одна из этих двух реакций не будет происходить с заметной скоростью вследствие того, что выделение водорода сопровождается перенапряжением, точно так же, как и в случае выделения водорода при электролизе. Условия выделения водорода при растворении металла в этом отношении не отличаются от условий процесса катодного выделения водорода, и один и тот же медленный процесс, каким бы он ни был, является промежуточной стадией в обоих случаях. Перенапряжение водорода со на свинце и цинке при небольших плотностях тока соответственно равно около 0 6 и 0 7 в, и из этого в согласии с рассуждениями, приведенными на стр. Так как указанные потенциалы значительно отрицательнее стандартных потенциалов этих металлов, а именно - 0 12 и-0 75 в, то водород выделяться не будет. При увеличении концентрации ионов водорода потенциал выделения водорода становится положительнее, и поэтому стремление металла к переходу в раствор должно увеличиваться. Таким образом, потенциал заметного выделения водорода на цинковом катоде будет равен около - 0 7 в. Это значение так близко к значению потенциала растворения цинка, что следовало бы ожидать медленного растворения цинка в сильно кислых растворах. [39]
Следующим шагом в дальнейшем усовершенствовании явилось оголение большой части стального дна для использования его в качестве токоподвода к ртутному катоду и закрепление гуммировки по краям дна прижимными планками, как это схематично показано на рис. 46 0 ( стр. Необходимость в прижимных стальных планках вызвана тем, что не закрепленная механически гуммировка постепенно отрывается и вздувается в процессе катодного выделения водорода, постепенно распространяющегося под слой гуммировки. [40]
Излагается теория двойного слоя на границе металл-раствор и механизм возникновения скачка потенциала на этой границе. Обсуждается поведение металлических электродов в условиях протекания внешнего тока на основе общей теории кинетики электродных процессов. Детально рассматриваются кинетические закономерности процессов катодного выделения водорода, электрохимического восстановления кислорода и ионизации металлов. Выведены выражения, определяющие коррозионное поведение металлов в условиях их саморастворения для случая идеально однородной поверхности и при ее дифференциации на анодную и катодную зоны. [41]
Для ртутного электрода наклон поляризационной кривой выделения водорода составляет примерно 116 мв. Рекомбина-ционная теория без дополнительных предположений не позволяет также объяснить зависимость перенапряжения от рН и состава раствора. Поэтому рекомбинационная теория неприменима к процессу катодного выделения водорода на ртутном электроде. [42]
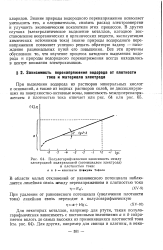 |
Полулогарифмическая зависимость между электродной поляризацией ( потенциалом электрода. [43] |
Знание природы водородного перенапряжения позволяет уменьшить его, а следовательно, снизить расход электроэнергии и улучшить экономические показатели этих процессов. В других случаях ( электролитическое выделение металлов, катодное восстановление неорганических и органических веществ, эксплуатация химических источников тока) знание природы водородного перенапряжения позволяет успешно решать обратную задачу - нахождение рациональных путей его повышения. Все эти причины обусловили то, что изучение процесса катодного выделения водорода и природы водородного перенапряжения всегда находилось в центре внимания электрохимиков. [44]
Из уравнений ( ХХ-29) и ( ХХ-33) следует также, что перенапряжение должно уменьшаться под влиянием всех факторов, увеличивающих ток обмена. Наиболее важными из них следует считать природу металла и растворителя. Для качественной оценки влияния этих факторов на величину электрохимического перенапряжения весьма удобным оказался метод потенциальных кривых, предложенный Гориучи и Поляни в 1935 г. С помощью этого метода Го-риучи и Поляни дали описание процесса катодного выделения водорода и получили качественно совпадающую с опытом зависимость между электрохимическим перенапряжением и плотностью тока. Здесь в качестве примера будет рассмотрено выделение водорода из кислых растворов. Электрохимический акт отвечает в данном случае переходу протона из состояния гидратированного иона в состояние атома водорода, адсорбированного металлом. Кривая АВД передает изменение свободной энергии гидратированного протона как функцию расстояния между протоном и молекулой воды. Потенциальная кривая NCBF отвечает увеличению ( или уменьшению) свободной энергии системы Н - М с изменением расстояния между адсорбированным атомом водорода и поверхностью металла. [45]
Страницы: 1 2 3 4