Процесс - катодное выделение - водород
Cтраница 2
Таким образом, большинство данных полученных при изучении процесса катодного выделения водорода па платине, указывает на замедленность рекомбинации как на наиболее вероятную причину появления перенапряжения. В то же время имеются известные основания утверждать, что при отравлении платины ( или при значительных отклонениях ее потенциала от равновесного) механизм электролитического выделения водорода может измениться и замедленной стадией будет разряд или электрохимическая десорбция. В связи с неоднородностью поверхности гладкой платины не исключена также возможность различного механизма выделения водорода на разных ее участках. На губчатой платинированной платине вследствие ее высокой каталитической активности весь сдвиг потенциала, наблюдающийся при наложении тока, вызван, вероятно, лишь замедленным удалением молекулярного водорода из примыкающего к электроду раствора. [16]
Теория замедленного разряда была разработана первоначально применительно к процессу катодного выделения водорода. [17]
Теория замедленного разряда была разработана первоначально применительно к процессу катодного выделения водорода. В настоящее время получен большой фактический материал, указывающий на ее приложимость к самым различным электрохимическим процессам. [18]
Таким образом, большинство данных, полученных при изучении процесса катодного выделения водорода на платине, указывает на замедленность рекомбинации как на наиболее вероятную причину появления перенапряжения. В то же время имеются известные основания утверждать, что при отравлении платины ( или при значительных отклонениях ее потенциала от равновесного) механизм электролитического выделения водорода может измениться и замедленной стадией будет разряд или электрохимическая десорбция. В связи с неоднородностью поверхности гладкой платины не исключена также возможность различного механизма выделения водорода на разных ее участках. На губчатой платинированной платине вследствие ее высокой каталитической активности весь сдвиг потенциала, наблюдающийся при наложении тока, вызван, вероятно, лишь замедленным удалением молекулярного водорода из примыкающего к электроду раствора. [19]
 |
Схема перехода водорода. [20] |
Таким образом, большинство опытных данных, полученных при изучении процесса катодного выделения водорода на платине, указывает на замедленность рекомбинации как на наиболее вероятную причину появления перенапряжения. В то же время имеются известные основания утверждать, что при отравлении платины ( или при значительных отклонениях ее потенциала от равновесного) механизм электролитического выделения водорода может измениться и замедленной стадией будет разряд или электрохимическая десорбция. В связи с неоднородностью поверхности гладкой платины не исключена также возможность различного механизма выделения водорода на разных ее участках. На губчатой - платинированной платине вследствие ее высокой каталитической активности весь сдвиг потенциала, наблюдающийся при наложении тока, вызван, вероятно, лишь замедленным удалением молекулярного водорода из примыкающего к электроду раствора. [21]
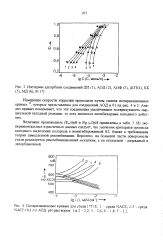
Из экспериментальных и расчетных данных следует, что значения критериев процесса катодного выделения водорода в неингибированной КС ближе к требованиям теории замедленной рекомбинации. Вероятно, на большей части поверхности стали реализуется рекомбинационный механизм, а на остальной - разрядный и десорбционный. [23]
Уравнения реакций (19.1), (19.2) и (19.3) представляют собой суммарное выражение процесса катодного выделения водорода при различных условиях электролиза. Этот процесс состоит из ряда по-следовательных стадий и может протекать по различным путям в зависимости от конкретных условий. Первая стадия - доставка к поверхности электрода частиц, служащих источником получаемого катодного водорода, протекает в данном случае без существенных торможений. [24]
Уравнения реакций (19.1), (19.2) и (19.3) представляют собой суммарное выражение процесса катодного выделения водорода при различных условиях электролиза. Этот процесс состоит из ряда последовательных стадий и может протекать по различным путям в зависимости от конкретных условий. Первая стадия - доставка к поверхности электрода частиц, служащих источником получаемого катодного водорода, протекает в данном случае без существенных торможений. [25]
Из экспериментальных и расчетных данных ( см. табл. 1) следует, что значения критериев процесса катодного выделения водорода в неингибированной среде ближе к требованиям теории замедленной рекомбинации. [26]
Уравнения реакций ( 612), ( 613) и ( 614) представляют собой суммарное выражение процесса катодного выделения водорода. Этот процесс состоит из ряда последовательных стадий и может протекать по различным путям в зависимости от условий электролиза. Первая стадия - доставка к поверхности электрода частиц, служащих источником катодного водорода, протекает в данном случае без существенных торможений. [27]
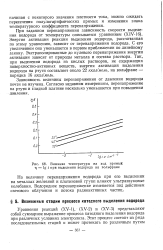 |
Влияние температуры на ход прямых т - lg i при выделении водорода на вольфраме. [28] |
Уравнения реакций ( XV-1), ( XV-2) и ( XV-3) представляют собой суммарное выражение процесса катодного выделения водорода при различных условиях электролиза. [29]
Уравнения реакций ( ХХ-1), ( ХХ-2) и ( ХХ-3) представляют собой суммарное выражение процесса катодного выделения водорода при различных условиях электролиза. Этот процесс состоит из ряда последовательных стадий и может протекать по различным путям в зависимости от конкретных условий. Первая стадия - доставка к поверхности электрода частиц, служащих источником получаемого катодного водорода, протекает в данном случае без существенных торможений. [30]
Страницы: 1 2 3 4