Введение - электроноакцепторный заместитель
Cтраница 1
Введение электроноакцепторных заместителей стабилизирует сопряженное основание и повышает силу кислоты. [1]
Введение электроноакцепторных заместителей в ферроцен затрудняет окисление. [2]
 |
Изменение потенциальной энергии при отрыве атома водорода несольватированным ( / и сольва-тированным ( 2 атомами хлора. [3] |
Введение электроноакцепторных заместителей приводит к противоположному эффекту. [4]
Введение электроноакцепторных заместителей в молекулу хлоргидрина I должно увеличивать кислотность последнего, что приведет к росту К. [5]
Введение электроноакцепторного заместителя дестабилизирует исходный б-комплекс, и переходное состояние для стадии отрыва протона смещается в сторону исходного, степень растяжения С - Н - связи в переходном состоянии уменьшается. Это должно приводить к уменьшению величины изотопного эффекта, что и наблюдается в действительности. [6]
При введении электроноакцепторных заместителей увеличивается кислотность атомов водорода, связанных с атомом углерода. Так, при действии сильных оснований на хлороформ образуется неустойчивый карбанион - СС13 ( ср. К этому можно добавить, что значения рКа HCF3 и НС ( СЕ3) 3 равны л; 28 и 11 соответственно. Еще большее влияние оказывают заместители, которые могут способствовать делокализации отрицательного заряда и обладают, кроме того, электроноакцептор-ным индуктивным эффектом. Так, значения р / Са MeCN, MeCOMe и MeNO2 равны 25, 20 и 10 2 соответственно, В случае CH3NO2 соответствующий карбанион - CH2NO2 может быть получен при действии - OEt в ЕЮН или даже - ОН в Н2О ( ср. [7]
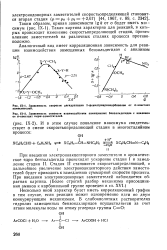 |
Зависимость скорости дегидратации 2-фенилтриарилкарбинолов от о-констант заместителей.| Зависимость скорости взаимодействия замещенных бензальдегидов с анилином от о-констант пара-заместителей. [8] |
При введении электроноакцепторного заместителя в ароматическое ядро бензальдегида происходит ускорение стадии I и замедление стадии II. Стадия II становится скоростьопределяющей, и дальнейшее увеличение электроноакцепторного действия заместителей будет приводить к замедлению суммарной скорости процесса. При введении электронодонорных заместителей наблюдается обратная картина. Более строгий разбор механизма присоединения аминов к карбонильной группе проведен в гл. [9]
При введении электроноакцепторных заместителей скорость стадии присоединения увеличивается, а скорость дегидратации уменьшается, и последняя стадия становится наиболее медленной. Как мы уже разобрали, в этом случае влияние заместителей на скорость реакции невелико. [10]
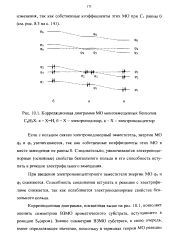 |
Корреляционная диаграмма МО монозамещенных бензолов СбН5Х. а - ХН, б - X - электронодонор, в - X - электроноакцептор. [11] |
При введении электроноакцепторного заместителя энергии МО ф2 и Фз снижаются. Способность соединения вступать в реакции с электрофилами снижается, так как ослабляются электронодонорные свойства бензольного кольца. [12]
При введении электроноакцепторного заместителя энергии молекулярных орбиталей ф2 и ф5 снижаются. Снижается и способность соединения вступать в реакции с электрофилами, так как ослабляются электронодо-норные свойства бензольного кольца. [13]
По-видимому, введение электроноакцепторного заместителя ( атома галогена) к а-углеродному атому приводит к существенному увеличению протонной подвижности соответствующего атома водорода. [14]
Как влияет введение электронодонорных и электроноакцепторных заместителей на свойства красителей. Как повлияют они на спектры поглощения. [15]
Страницы: 1 2 3 4