Введение - электроноакцепторный заместитель
Cтраница 3
Данные табл. 1 показывают, что при введении электроноакцепторных заместителей величина Кд уменьшается, а при введении объемистых групп увеличивается. [31]
Как видно из табл. 1 и 2, введение электроноакцепторных заместителей к карбинольному атому углерода, увеличивает протоно-донорную способность ОН группы. Окружение атома фосфора оказывает незначительное влияние па кислотность ОН группы. [32]
Активность арилгалогенидов возрастает в ряду: Cl Br I Введение электроноакцепторных заместителей ( NO2, CH3CO), осо бенно в орго-положение к атому галогена, способствует реакции Процесс проводят, нагревая арилгалогенид или его раствор с 3 - 10-кратным избытком порошка меди. В качестве растворител5 используют нитробензол, алифатические и алициклические углево дороды, пиридин, хинолин и другие, но наиболее часто диметил-формамид. Последний позволяет снизить температуру, сократит. [33]
 |
Зависимость реакционности замещенных стиролов по отношению к полистирольному радикалу от константы а Гаммета для заместителя. [34] |
Положительное значение р указывает на увеличение скорости реакции при введении электроноакцепторных заместителей. [35]
Сравнивая полученные значения / гэф, можно заключить, что введение электроноакцепторных заместителей в ароматическое кольцо изонитро-зобензоилацетона приводит к увеличению скорости реакции. Полученные результаты позволяют объяснить преимущественное образование и-нит-розофенолов при конденсации изонитрозобензоилацетонов. Поскольку карбонильная группа, связанная с метильной группой, более реакцион-носпособна, чем фенилкарбонильная, конденсация с ацетоном начинается по этой группе. [36]
Было показано, что понижение полярности растворителя, повышение температуры и введение электроноакцепторных заместителей способствует образованию азидной формы. [37]
Положительный знак р свидетельствует о том, что реакция облегчается при введении электроноакцепторных заместителей в ароматическое ядро. [38]
Нам представляется вероятным, что именно сольватационные эффекты ответственны за увеличение энтальпии активации при введении электроноакцепторных заместителей в молекулу бензилгалоге-нида в приводимой ранее ( с. В этой реакции заместители влияют лишь на перпендикулярную координату. Введение в субстрат электроноакцепторных групп приводит к увеличению порядков реагирующих связей и к сжатию переходного состояния, вызывающему десольватацию обоих нуклеофилов. [39]
В случае фенолов ситуация иная: для слабых кислот АН 0, но при введении электроноакцепторных заместителей АН становится меньше, а для пикрниовой кислоты процесс уже слабо экзотермичен. Одновременно и энтропия становится менее отрицательной. Это связано с тем, что электроноакцепторные заместители, полярные по своей природе, делают молекулу недиссоциированной кислоты более полярной ( более похожей на диссоциированные ионы), и поэтому различие между недиссоциированной кислотой и ионами в способности разупорядочивать или упорядочивать структуру воды уменьшается. [40]
Формально эта реакция представляет собой отщепление молекулы воды; для осуществления реакции требуется активирование карбоксильной группы введением электроноакцепторного заместителя X. [41]
При введении электронодонорных заместителей интенсивность поглощения несколько увеличивается, но, в общем, как и при введении электроноакцепторных заместителей, изменяется мало. [42]
Положительный заряд на реакционном центре в активированном комплексе существенно ниже, чем в исходном карбонильном соединении, и введение электроноакцепторных заместителей в большей степени дестабилизирует исходное состояние, чем переходное. В результате скорость реакции должна возрастать. [43]
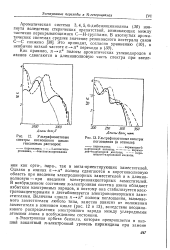 |
Ультрафиолетовые спектры поглощения ( в этаноле. [44] |
Однако в азинах л - л полосы сдвигаются в коротковолновую область при введении электродонорных заместителей и в длинноволновую - при введении электроноакцепторных заместителей. В возбужденном состоянии л-электронная система азина обладает избытком электронных зарядов, и поэтому она стабилизуетсяэлек-троноакцепторными и дестабилизуется электронодонорными заместителями. Величина сдвига п - л полосы поглощения, вызываемого заместителем любого типа, заметно зависит от положения заместителя в азиновом цикле ( рис. 12 и 13), вследствие неодинакового распределения электронного заряда между углеродными атомами азина в возбужденном состоянии. [45]
Страницы: 1 2 3 4