Введение - электронодонорный заместитель
Cтраница 1
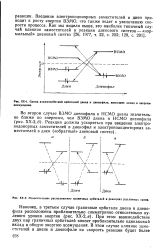 |
I. Схема взаимодействий орбиталей диена и диенофила. вносящих вклад в энергию возмущения. [1] |
Введение электронодонорных заместителей в диен приводит к росту энергии ВЗМО, что также ведет к увеличению скорости процесса. [2]
Введение электронодонорных заместителей должно вызывать обратный эффект. Донорные свойства ме-тильной группы сильнее проявляются в пара -, чем в мета-положении, а акцепторные свойства хлора - в мета-положении. [3]
Введение электронодонорных заместителей оказывает незначительное влияние на положение га, л - состояний, но может привести к очень сильному донижению энергии л, л - состояний вследствие сопряжения с ароматическим ядром. [4]
Введение электронодонорных заместителей дестабилизирует сопряженное основание и снижает силу кислоты. [5]
При введении электронодонорных заместителей интенсивность поглощения несколько увеличивается, но, в общем, как и при введении электроноакцепторных заместителей, изменяется мало. [6]
При введении электронодонорных заместителей в стильбеновый фрагмент молекулы абсолютный квантовый выход флуоресценции существенно уменьшается по сравнению с незамещенными соединениями. По-видимому, это связано с тем, что у фенилэтиленовых производных дифенилоксазола и дифенйлоксадиазола длинноволновая полоса, ответственная за люминесценцию, является полосой переноса заряда с фенилоксазольного или фенилоксадиазольного фрагмента молекулы на стильбеновый. Введение в стирильный радикал электронодонорных заместителей противодействует такому электронному смещению, уменьшая сопряжение в молекуле и увеличивая вероятность безызлучательных потерь энергии электронного возбуждения. [7]
При введении электронодонорных заместителей в ароматическое ядро стабилизируется образующийся катион. [8]
При введении электронодонорных заместителей в ароматическое ядро арилсульфохлорида стабильность ионной пары увеличивается, и стадия сульфонирования становится более эндотермич-ной. Это приводит к тому, что переходное состояние приближается по строению к о-комплексу. Таким образом, введение электронодонорных заместителей должно приводить к уменьшению вероятности орго-замещения, что и имеет место в действительности. [9]
При введении электронодонорных заместителей в диен скорость реакции диенового синтеза также увеличивается. [10]
При введении электронодонорных заместителей в ароматическое ядро стабилизируется образующийся катион. [11]
При введении электронодонорных заместителей в диен скорость реакции диенового синтеза также увеличивается. [12]
При введении электронодонорных заместителей наблюдаются аналогичные закономерности. [13]
Такое сильное влияние введения электронодонорного заместителя в пара-положение ароматического ядра н-карбамоил - Н - фенил-гидроксиламина на ход перегруппировки, по-видимому, можно объяснить созданием в ароматическом кольце избыточной электронной плотности, что может способствовать смещению электронной плотности в направлении от ядра к атому азота гядроксилашна. [14]
Увеличение реакционности при введении электронодонорных заместителей указывает на то, что скорость реакции определяется 1 - й стадией. [15]
Страницы: 1 2 3 4