Прочность - связь - электрон
Cтраница 1
Прочность связи электрона в атоме измеряется работой, которую надо совершить, чтобы удалить его на бесконечное расстояние, при котором взаимодействие между атомом и электроном было бы практически равным нулю. Эти же условия распространяются и на комплекс атомов. [1]
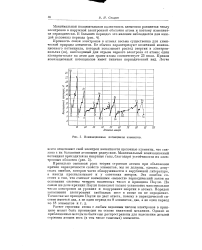 |
Ионизационные потенциалы элементов. [2] |
Прочность связи электронов в атомах весьма существенна для химической природы элементов. Ее обычно характеризуют величиной ионизационного потенциала, который показывает расход энергии в электрон-вольтах ( эв), необходимый для отрыва первого электрона от атома; один электрон-вольт на атом для грамм-атома соответствует 23 ккал. Кривая ионизационных потенциалов имеет типично периодический вид. [3]
Прочность связи электронов внешнего слоя с ядром увеличивается. [4]
Прочность связи электронов внешнего слоя с ядром уменьшается. [5]
Характеризует прочность связи электрона в атомной системе. ИОНИЗАЦИЯ, превращение атомов или молекул в положит, ионы в результате отрыва одного или неск. Энергия, необходимая для отрыва электрона, наз. Нейтральные атомы и молекулы могут в особых случаях присоединять электроны, образуя отрицат. [6]
Мерой прочности связи электронов в атомах является величина энергии ионизации, или ионизационного потенциала ( гл. Очевидно, что восстановительная способность металлов связана с величиной энергии ионизации их атомов. Наименьшие значения ионизационного потенциала у щелочных металлов, которые и являются самыми энергичными восстановителями. [7]
Мерой прочности связи электрона в атоме может служить потенциал ионизации атома ( см. гл. [8]
Влияние на прочность связи электронов с ядром оказывает также взаимное отталкивание электронов одного и того же оюя и в особенности одной и той же орбитали. [9]
Влияние на прочность связи электронов с ядром оказывает также взаимное отталкивание электронов одного и того же слоя и в особенности одной и той же орбитали. [10]
Влияние на прочность связи электронов с ядром оказывает также взаимное отталкивание электронов одного и того же слоя и, в особенности, одной и той же орбитали. [11]
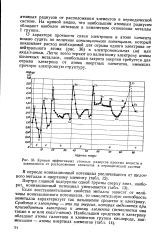 |
Кривая эффективных атомных радиусов простых веществ в зависимости от расположения элементов в периодической системе. [12] |
О характере прочности связи электронов в атоме элемента можно судить по величине ионизационного потенциала, который показывает расход необходимой для отрыва одного электрона от нейтрального атома ( рис. 36) в электроновольтах ( эв) или ккал / г-атом. Легче всего теряют по валентному электрону атомы щелочных металлов, наибольшая затрата энергии требуется для отрыва электрона от атома инертных элементов, имеющих прочную электронную структуру. [13]
Z, то прочность связи электрона ( равная - Enl) как функция п для сложного А. [14]
Z, то прочность связи электрона ( равная - й п) как функция п для сложного А. [15]
Страницы: 1 2 3 4