Псевдокислота
Cтраница 2
Представление диссоциации псевдокислот в виде енолизации имеет важные последствия для рассмотрения присоединения енола или енолята к карбонильной группе: как металл [ в схеме (6.45) ], так и водород гидроксильной группы [ в схеме (6.46) ] могут при определенных обстоятельствах вступать в хелатообразование с присоединяемой карбонильной компонентой. [16]
Реакции присоединения псевдокислот называют реакциями присоединения по Михаэлю. Эти реакции очень важны, так как с их помощью в одной стадии удается осуществить присоединение нескольких атомов углерода. [17]
Характерным для псевдокислот является и то, что их нейтрализация не является мгновенной реакцией, а требует времени. Истинные кислоты мгновенно нейтрализуются основаниями, так как здесь происходит взаимодействие между ионами. Нитросоединения, наоборот, медленно растворяются в щелочах; до образования щелочных солей в них должно произойти отщепление в виде протона атома водорода, находящегося при том же С-атоме, что и нитрогруппа, в результате чего возникает ациф орма. Эта перегруппировка является реакцией, требующей известного времени, и лишь по мере того как она протекает, становится возможной нейтрализация. [18]
Характерным для псевдокислот является и то, что их нейтрализация не является мгновенной реакцией, а требует времени. Истинные кислоты мгновенно нейтрализуются основаниями, так как здесь происходит взаимодействие между ионами. Нитросоединения, наоборот, медленно растворяются в щелочах; до образования щелочных солей в них должно произойти отщеплемте и впте протона атома водорода, находящегося при ч ом же С-атоме, что и питрогруппа, в результате чего возникает ациформа. Эта перегруппировка является реакцией, требующей известного времени, и лишь по мере того как она протекает, становится возможной нейтрализация. [19]
Реакции с псевдокислотами называют присоединением поМихаэлюв самом широком смысле. [20]
Ясно, что псевдокислоты попадают по номенклатуре Льюиса в число вторичных кислот, однако новое выражение гораздо шире, чем старое, которое, естественно, распространялось лишь на водородные кислоты. Большое значение имеет, однако, вопрос, не удастся ли нам объяснить поведение вторичных кислот и оснований путем обобщения предложенной Ганчшем теории таутомерии псевдокислот и оснований. Ответом на это будет, повидимому, определенное да. Поясним это несколькими примерами. [21]
Ганч перечислил признаки псевдокислот и описал некоторые методы, позволяющие установить принадлежность вещества к их числу. Например, вещество является псевдокислотой, если нейтрализация его щелочью не происходит мгновенно, а требует времени. [22]
Например, если псевдокислоту количественно перевести в анион с помощью натрия в инертном растворителе, то отщепляющийся протон за счет реакции окисления - восстановления переходит в газообразный водород, поэтому не образуется протоннрованное основание ВН. В таком случае невозможна реакция описанного типа. [23]
Безводный нитроформ является псевдокислотой; водные растворы его обладают интенсивной желтой окраской, присущей и солям нитроформа. [24]
Безводный нитроформ является псевдокислотой; водные растворы его обладают интенсивной желтой окраской, присущей и солям нитрофоргла. [25]
Какие соединения называются псевдокислотами. Чем они отличаются от истинных кислот. Какой из изомеров ароматических нитросоединений состава C H7NO2 является псевдокислотой. [26]
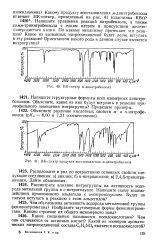 |
ИК-спектр ж-динитробензола. [27] |
Какие соединения называются псевдокислотами. Чем они отличаются от истинных кислот. Какой из изомеров ароматических нитросоединений состава C7HjNO2 является псевдокислотой. [28]
Этим объясняется происхождение термина псевдокислота. Аци-форма ведет себя как обычная кислота. Считалось, что карбокислота, сама не являясь настоящей кислотой, проявляет кислотные свойства благодаря способности давать а и-форму. С точки зрения современных представлений о кислотах и основаниях такой ход рассуждений не выдерживает критики. [29]
Альдольные аддукты представляют собой псевдокислоты; при действии на них основания-катализатора происходит быстрое отщепление протона и образуются анионы Ilia и IVa. От этих анионов отщепляется ион гидроксила ( стадия, определяющая скорость), и возникает сопряженная ненасыщенная система. [30]
Страницы: 1 2 3 4