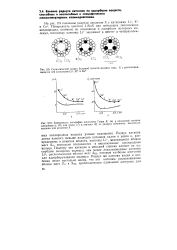
Радиус - катион
Cтраница 1
Радиусы катионов определяют форму и размеры их координационных полиэдров, образуемых атомами кислорода, которые одновременно входят в состав кремнийкислородных тетраэдров. [1]
Радиусы катионов и анионов обычно отличаются между собой, а так как коэффициент В зависит от радиуса, то и скорости их движения в электрическом поле различны. [2]
Радиус катиона Li меньше радиуса катиона К и соотношение величин энергий ионизации и гидратации для лития оказывается таким, что у него в водном растворе отнять электрон легче, чем у атома калия. [3]
Радиус катиона лития намного меньше радиусов катионов калия и цезия и, распределяясь в решетке цеолита, катионы 1Л, находящиеся вблизи мест 5ц, несколько втягиваются в шеетичленные кислородные кольца. Поэтому эти катионы в меньшей степени влияют на адсорбцию полярных молекул, чем менее локализованные катионы Li, расположенные вблизи мест 5щ, которые наиболее доступны для адсорбирующихся молекул. [5]
Если радиус центрального катиона меньше 0 8 А, то гидроксиды этих катионов должны функционировать амфотерно, так как работы диссоциации по Основному и кислотному типу близки друг к другу. [6]
Увеличение радиуса катиона ( переход от синтетического Li-и Na-фожазита к Rb - и Cs-фожазиту уменьшает теплоту адсорбции эфира и увеличивает теплоту адсорбции к-пентана. Разница между ними уменьшается почти в два раза. [7]
Влияние радиуса катиона на предел температуростойкости ( по сопротивлению разрыву) резин с ионными связями. [8]
Соотношение радиусов катиона и аниона ( ПУЕ / ГХ) является фактором, определяющим тип кристаллической структуры. На рис. 4.3 показаны наиболее распространенные структуры для соединений типа MX, а в табл. 4.3 - значения Гм / Гх, при которых реализуется каждая из этих структур. [9]
Влияние радиуса катионов фона на скорость электрохимических процессов восстановления впервые было исследовано в работах Герасименко и Слендика [1] и Н. А. Изгарышева и X. Герасименко и Слендик при изучении влияния катионов щелочных и щелочноземельных металлов на восстановление водорода нашли, что скорость выделения водорода в присутствии хлоридов щелочных металлов при переходе от лития к цезию уменьшается примерно в полтора раза. Такого же рода эффекты описаны в работах Н, А. [10]
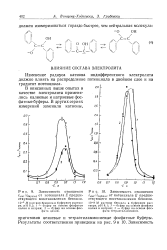 |
Зависимость отношения inuc / impanc от потенциала Е предшествующего восстановления бензила. [11] |
Изменение радиуса катиона индифферентного электролита должно влиять на распределение потенциала в двойном слое и на градиент потенциала. [12]
Если сопоставить радиусы катионов с радиусами изо-электронных с ними атомов инертных газов, то оказывается, что потеря электронов влияет на размеры в еще большей степени, чем их присоединение. Качественно можно указать на две причины этого явления. Потеря электронов увеличивает отношение заряд ядра / число электронов, так что остающиеся электроны оказываются более прочно связанными; кроме этого ( что еще более существенно) при ионизации исчезает целая квантовая оболочка. Как уже указывалось раньше, число электронов в данной незаполненной оболочке сравнительно мало влияет на размеры атома или иона; важно лишь то, что в данной оболочке вообще имеется некоторое число электронов. Однако данные, приведенные на рис. 21 и в двух изоэлектронных рядах, указывают на важность влияния заряда. [13]
Чем больше радиус катиона, тем меньшее количество частиц ( ионов) при прочих равных условиях укладывается в поверхностном слое соли и, следовательно, тем меньше будет притяжение их ионами, находящимися внутри расплава. [14]
Как относятся радиусы катиона и аниона к радиусу соответствующего электронейтрального атома. [15]
Страницы: 1 2 3 4