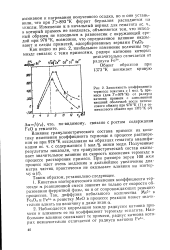
Радиус - катион
Cтраница 4
Наблюдается корреляция между радиусом катиона примеси и влиянием ее на коэффициент термоэдс гематита. [47]
Естественно, что если радиус катиона превышает радиус соответствующей пустоты, то анионы не могут находиться в соприкосновении друг с другом и расстояния между ними соответственно увеличиваются, что влечет за собой увеличение размеров ячейки. [48]
Маделунга невелика, а радиусы катионов не слишком малы, абсолютное значение левой части уравнения оказывается меньше 627 кДж - моль 1, и, следовательно, величина АЯ0 ( МР) - АЯ0 ( МОл / 2) отрицательна. Отсюда следует вывод о более высокой стабильности фторида. [49]
Во втором столбце приведены радиусы катионов дополнительных солей, полученные из кристаллографических данных. Хотя ион тиоцианата входит в состав всех дополнительных солей, последовательность изменения величины а для различных солей не совпадает с соответствующей последовательностью величин кристаллографических радиусов и, кроме того, изменяется в зависимости от природы насыщающей соли. Таким образом, среднее значение величины а является функцией обеих солей н не характеризует ни одну из них в отдельности. Этот вывод относится не только к системам типа кобальтаамминотио-цианатов, поскольку аналогичные результаты были получены Хлупеком, Данегп и Данешовой также для систем, состоящих из иодата церия или иодата кальция в присутствии различных солей, хотя в этих случаях колебания величины а не были столь велики. [50]
Во втором столбце приведены радиусы катионов дополнительных солей, полученные из кристаллографических данных. Хотя ион тпоцианата входит в состав всех дополнительных солей, последовательность изменения величины а для различных солей не совпадает с соответствующей последовательностью величин кристаллографических радиусов и, кроме того, изменяется в зависимости от природы насыщающей соли. Таким образом, среднее значение величины а является функцией обеих солей и не характеризует ни одну из них в отдельности. Этот вывод относится не только к системам типа кобальтаамминотио-цианатов, поскольку аналогичные результаты были получены Хлупеком, Дансш и Данешовой также для систем, состоящих из иодата церия или иодата кальция в присутствии различных солей, хотя в этих случаях колебания величины а не были столь велики. [51]
При этом с ростом радиуса катиона он падает, & с ростом заряда растет. [52]
Известно, что сумма радиусов катиона и аниона практически не отличается ( в пределах сотых долей ангстрема) от суммы кова-лентных радиусов соответствующих атомов. А-В в контактную ионную пару А В - происходит без существенного сдвига тяжелых атомов, и его энергия активации практически целиком определяется реорганизацией растворителя. [53]
 |
Отношения ионных радиусов и положение катионов в плотноупакованной анионной решетке. [54] |
При дальнейшем увеличении отношения радиусов катиона и аниона, т.е. при условии гк / га 0 414, анионы расталкиваются катионами, что уменьшает дестабилизующие анионно-анионные контакты при одновременном сохранении стабилизующих катионно-анионных контактов. В ионных кристаллических решетках, для которых отношение гк / га находится в пределах от 0 414 до 0 732, катионы обычно находятся в октаэдрических дырках. Если отношение гк / г превышает 0 732, то плотноупакованная структура анионов перестает быть устойчивой. Вместо этого более устойчивой становится простая кубическая структура. В такой структуре катион находится в контакте сразу с восемью анионами, что увеличивает число стабилизующих катионно-анионных контактов. В табл. 22.7 указаны значения отношения гк / га, по которым можно судить о наиболее вероятном размещении катионов в решетке из более крупных анионов. [55]
Радиус катиона Li меньше радиуса катиона К и соотношение величин энергий ионизации и гидратации для лития оказывается таким, что у него в водном растворе отнять электрон легче, чем у атома калия. [56]
Следовательно, при уменьшении радиуса примесного катиона значение эффективного коэффициента уменьшается. [57]
Это отличие корродируется с увеличением радиуса катиона. [58]
Страницы: 1 2 3 4