Величина - водородное перенапряжение
Cтраница 1
Величина водородного перенапряжения снижается с повышением температуры. [1]
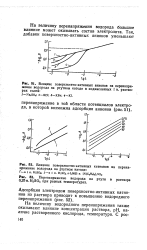
Величина водородного перенапряжения снижается с повышением температуры. Это видно из фиг. [2]
 |
Зависимость перенапряжения водорода на ртутном электроде рН от раствора при плотности тока 1 - 10 - 4 а / см2. [3] |
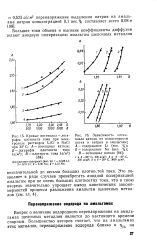
Величина водородного перенапряжения снижается с повышением температуры. Температурный коэффициент для металлов с высоким значением водородного перенапряжения ( например, для ртути, свинца, кадмия, цинка) при средних значениях плотности тока ( порядка 10 - 3 - - 10 - 5 а / см) составляет 2 - 4 мв на 1 град. [4]
Величина водородного перенапряжения играет важную роль в самых различных электрохимических явлениях. Величина и природа водородного перенапряжения влияют на протекание многих электрохимических процессов. Так, катодное восстановление неорганических и органических веществ, электроосаждение металлов и их самопроизвольное электрохимическое разрушение протекают неодинаково, а зависят от механизма выделения водорода на металле. [5]
На величину водородного перенапряжения также оказывают влияние концентрация раствора, рН, наличие растворенного кислорода, температура. [7]
Вопрос о величине водородного перенапряжения на амальгамах щелочных металлов является до настоящего времени спорным. [9]
Скорость выделения водорода при саморазряде в сильной степени зависит от величины водородного перенапряжения. [10]
Максимально допустимый потенциал, создаваемый средствами электрозащиты, не должен превышать минус 1 2 в, так как превышение отрицательного потенциала выше величины водородного перенапряжения приводит к выделению водорода на поверхности трубы и отслаиванию изоляции от трубы. [11]
Изучая кинетику разложения амальгам щелочных и щелочно-земельных металлов, они показали, что щелочной металл, растворенный в ртути, существенно не влияет на величину водородного перенапряжения. [12]
Как было показано в работах А. И. Левина с сотрудниками, относительное распределение тока между обоими ионами определяется отношением их концентраций в растворе, а также величиной металлического и водородного перенапряжения. [13]
Теория медленного разряда в том виде, в каком она была изложена Фольмером, не учитывала строения границы электрод - раствор, потому не могла объяснить влияния состава электролита на величину водородного перенапряжения. Влияние строения двойного электрического слоя на кинетику электрохимических реакций впервые было принято во внимание А. Н. Фрумкиным, который показал, что, с одной стороны, силы электростатического взаимодействия между электродом и ионами вызывают изменение концентрации реагирующих ионов в зоне реакции, а с другой, - наличие двойного слоя сказывается на величине энергии активации электродного процесса. [14]
 |
Смещение потенциальной кривой. [15] |
Страницы: 1 2 3 4