Величина - энергия - активация - реакция
Cтраница 1
Величины энергий активации реакции ( 2) позволяют вычислить энергии связей в окисляющихся веществах. [1]
Величина энергии активации реакции ( 29) ( Е1 - Е - Е 74 5 ккал / моль) совпадает с величиной теплового эффекта ее. [2]
Величины энергий активации реакции ( 2) позволяют вычислить энергии связей в окисляющихся веществах. [3]
Величина энергии активации реакции в пламени Е, входящая в уравнение (4.18) для оценки величины Рекр для большинства горючих газовых смесей составляет 20 - 40 ккал / моль. [4]
Величины энергии активации реакции ( 2) могут быть оценены, исходя из величин энергий разрываемых связей С - Н QR-H при помощи соотношения Поляни. [5]
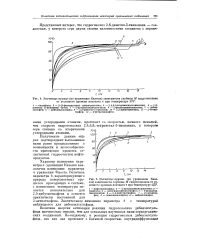 |
Расчетные кривые ( по уравнению Казеева зависимости глубины М гидрогенолиза от условного времени контакта т при температуре 375. [6] |
Величина энергии активации реакции гидрогенолиза дибензилсульфида значительно меньше, чем для остальных изученных нами сераорганиче-ских соединений. [7]
Величины энергий активации реакции отрыва мономера от радикала и реакции обрыва не были определены экспериментально, однако приближенные значения можно найти из других данных. Для Ер в литературе приводятся значения 4 4 и 6 3 ккал / моль. Если для Ер принять среднее значение 5 5, то для Ed получим 18 5 ккал / мо. Полная энергия активации фотодеполимеризации была определена для различных образцов полиметилметакрилата и оказалась равной 8 - 1 - 1 ккал / моль. [8]
 |
Энергия активации прямой и обратной реакции. [9] |
Величина энергии активации реакций горения газовых смесей находится в пределах Е от 85 до 170 Мдж / кмоль. [10]
Расхождение величин энергии активации реакции крекинга пропана, найденных в указанных двух работах, может служить любопытной иллюстрацией несовершенства динамического метода крекинга. [11]
Для величин энергий активации реакции диспропорционирования этильных радикалов найдены значения 0 8 и 1 45 ккал, при предполагаемых величинах; энергий активации реакции рекомбинации 0 и 0 65 ккал соответственно. Предэкспонен-ты получаются одинаковой величины для реакций диспропорционирования и рекомбинации и к тому же высокими, что представляется странным. [12]
Характеризуется величиной энергии активации реакции образования; перекиси. [13]
 |
Зависимость скорости ( и взаимодействия углерода ( мкмоль / см3 сек с СОа ( Х и Н2О ( О от температуры. [14] |
Между тем величина энергии активации реакции углерода с СО2 при нормальных давлениях весьма чувствительна к примесям как минерального, так и органического типа. Возможно, поэтому, что на результаты других опытов могло повлиять присутствие в угле небольших количеств тех или иных веществ, ускоряющих реакцию. [15]
Страницы: 1 2 3 4