Величина - энтальпие
Cтраница 1
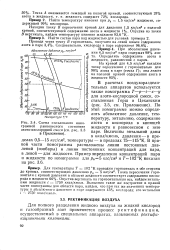 |
Схема пользования номограммой равновесного состояния азото-кислородной смеси ( в Приложении. [1] |
Величины энтальпий даны в ккал / кмоль, давления - в пределах 0 5 - 15 кгс / см2, температуры - в пределах 75 - 115 К. В правой части номограммы расположены линии постоянных давлений ( изобары) и линии постоянных концентраций для пара, в левой - для жидкости. [2]
Величина энтальпий ДЯ / ( № 4 25 - 105 Дж / моль, A / / ( Si) 3 7 - Ю5 Дж / моль и ДЯ / ( Сг) 3 3 - 105 Дж / моль; в парообразном состоянии эта величина наибольшая для Ni. Однако наиболее активным взаимодействием с компонентами остаточных газов отличается хром. Хром также наиболее активен при образовании карбидов. Никель, как известно, часто выступает при проведении химических реакций в качестве катализатора. [3]
Величины энтальпий разбавления обычно выражают в единицах энергии, отнесенных к единице массы находящегося в растворе растворенного вещества. [4]
Величины энтальпий испарения мононитроалканов, полученные в работе [201] по литературным данным о температурных зависимостях давлений пара, удовлетворительно воспроизводятся расчетным методом. [5]
Величины энтальпий сгорания веществ в газообразном состоянии ДН гор / г могут быть получены из величин ДНсгор ( Ж) прибавлением к ним величин АНИСП, где ДНИСП - - изменение энтальпии при испарении моля соответствующего вещества при температуре 25 С. Величины ДНИСП находят опытным путем или с использованием соответствующих эмпирических уравнений ( подробнее об этом см. раздел III данной книги, стр. [6]
Величины энтальпий образования веществ, количество которых существенно меньше величин энтальпий реакций, помещают в справочники и используют для расчетов энтальпий самых разнообразных реакций. [7]
Величины энтальпий растворения веществ в различных растворителях и энтальпий смешения и разбавления находят широкое использование в основном в двух направлениях. Во-первых, эти величины часто оказываются существенными для развития некоторых представлений в теории строения и химической термодинамике растворов. Во-вторых, очень часто приходится использовать эти величины при расчете энтальпий реакций на основе закона Гееса. [8]
Величины энтальпий образования ионов играют большую роль при изучении термодинамики и строения растворов. [9]
Используя величины энтальпий, рассчитать количеств теплоты, которое необходимо для нагревания 100 м3 этилена от О до 300 С при нормальном давлении. [10]
Используя величины энтальпий ( см. табл. 4 приложения), рассчитать количество теплоты, которое необходимо для нагревания 100 ж3 этилена от 0 до 300 С при нормальном давлении. [11]
Хотя величина энтальпий ионизации, как правило, дает основной, а часто подавляющий по величине вклад в энтальпию разбавления ассоциированных электролитов при расчете последней по уравнениям ( 3) и ( 6), для строгого расчета необходима также величина АЯпх, а при использовании уравнения ( 6) и АЯнедис. [12]
В величины энтальпий образования, стоящих в уравнении ( 137) справа, обычно входят очень большие зна-энтальпий перевода веществ из их устойчивого 25 С состояния в газ, а также энтальпия реакция образования сложного вещества из простых. [13]
Имея величины энтальпий образования ионов, можно, используя энтальпии растворения, рассчитывать энтальпии образования соединений, образованных этими ионами в любых комбинациях, поскольку энтальпия образования какого-либо иона в бесконечно разбавленном растворе не зависит от наличия в этом растворе других ионов. [14]
Содержащаяся здесь величина энтальпия активации АН описывает разницу между энтальпией исходной системы и переходного состояния. Различия в энтальпии по координате реакции могут быть следствием, например, потенциалов отталкивания и притяжения между атомами в случае различия межатомных расстояний. Величина АН дает также различие в сольватации или в кулоновской энергии при возникновении и исчезновении зарядов. [15]
Страницы: 1 2 3 4