Развитие - питтинговая коррозия
Cтраница 1
Развитие питтинговой коррозии происходит, только если в растворе концентрация галоидного иона, равная или превышающая критическую, зависит от природы металла или сплава, его термческой обработки, температуры раствора, характера других ионов и окислителей. Для сплавов Fe-Cr критическая концентрация хлор-ионов увеличивается при повышении содержания в сплаве хрома, а содержание никеля в сплаве практически не влияет на, ее величину. HCl NaCl при 25 С) наблюдается для чистого железа. [1]
Влияние температуры раствора на развитие питтинговой коррозии представляет большой интерес. Повышение температуры раствора может привести к изменению характера питтинговой коррозии стали. Например, Стрейчер наблюдал, что с повышением температуры раствора до 50 С положительное влияние добавок молибдена на стойкость стали к питтинговой коррозии полностью исчезает. С повышением температуры на нержавеющих сталях число питтингов резко возрастает, а их средняя и максимальная глубина остается практически постоянной. При 60 - 70 С на поверхности стали образуется много мелких питтингов, глубина которых не превышала 0 1 мм. Отсутствие изменения глубины питтинга объясняется увеличением числа центров, в которых сталь активируется. При этом ток катодной реакции восстановления окислителя распределяется на большее число анодов. Таким образом повышение температуры как и агрессивности раствора способствует постепенному переходу к развитию1 более общей коррозии. [2]
Что же касается скорости развития питтинговой коррозии, то по мере увеличения концентрации окислителя увеличивается скорость катодной реакции, что должно вызвать ускорение сопряженной анодной реакции, приводящей к проникновению коррозии в глубь металла. Однако это продолжается не беспредельно, ибо имеются условия для пассивации металла внутри питтингов, приводящие к исключительно неравномерной скорости развития отдельных питтингов. Начиная с определенной концентрации окислителя, плотность тока в большинстве питтингов достигает, очевидно, такой величины, которая уже достаточна для заметного торможения анодной реакции, а в некоторых из них - и для наступления анодной пассивности. В связи с последним и прекращается процесс в большинстве точек. [3]
Что же касается скорости развития питтинговой коррозии, то по мере увеличения, концентрации окислителя увеличивается скорость катодной реакции, что должно вызвать ускорение сопряженной анодной реакции, приводящей к проникновению коррозии в глубь металла. Однако это продолжается не беспредельно, ибо имеются условия для пассивации металла внутри питтингов, приводящие к исключительно неравномерной скорости развития отдельных питтингов. Начиная с определенной концентрации окислителя, плотность тока в большинстве питтингов достигает, очевидно, такой величины, которая уже достаточна для заметного торможения анодной реакции, а в некоторых из них - и для наступления анодной пассивности. В связи с последним и прекращается процесс в большинстве точек. [4]
Следует различать три стадии развития питтинговой коррозии: 1) возникновение питтинга; 2) рост питтинга; 3) репассивацию. При некоторых условиях процесс питтинговой коррозии может стабилизироваться на второй стадии. Третья стадия не всегда реализуется, но практически является наиболее важной, так как в результате репассивации прекращается рост питтинга. [5]
Рассмотрим электрохимические особенности возникновения и развития питтинговой коррозии в условиях саморастворения и при анодной поляризации. [6]
Поскольку однородная структура менее благоприятна для развития питтинговой коррозии, режим термической обработки должен обеспечить получение чисто аустенитной структуры. Термическая обработка, приводящая к выпадению карбидов и обеднению границ зерен хромом ( отпуск при 600 С для аустенитных сталей), сообщает стали повышенную склонность к питтинговой коррозии, и поэтому ее следует избегать. [7]
Поскольку однородная структура менее благоприятна для развития питтинговой коррозии, режим термической обработки должен обеспечить получение чисто аустенитной структуры. Термическая обработка, приводящая к выпадению карбидов и обеднению границ зерен хромом ( отпуск при 600 С для аустенитных сталей) / сообщает стали повышенную склонность к питтинговой коррозии, и поэтому ее следует избегать. [8]
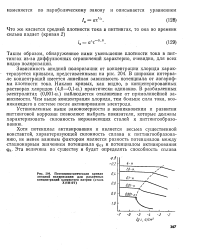 |
Потенциостатическая кривая. [9] |
Установленные выше закономерности в возникновении и развитии питтинговой коррозии позволяют выбрать показатели, которые должны характеризовать склонность нержавеющих сталей к питтингообразо-ванию. [10]
 |
Потенциостатическая кривая. [11] |
Установленные выше закономерности в возникновении и развитии питтинговой коррозии позволяют выбрать показатели, которые должны характеризовать склонность нержавеющих сталей к питтингообразо-ванию. [12]
Таким образом, пробой анодной пленки и развитие питтинговой коррозии на титане в растворах хлоридов средней концентрации практически могут осуществляться в результате воздействия внешнего анодного тока, при наложении которого достигаются любые положительные потенциалы. Необходимо также учитывать опасность пробивания анодной пленки галоидными ионами при осуществлении анодной защиты титана в кислых средах, содержащих ионы галоидов. В этом случае необходимы строгий контроль за потенциалом защищаемой конструкции и автоматическое его регулирование с целью поддержания потенциалов в безопасной области. [13]
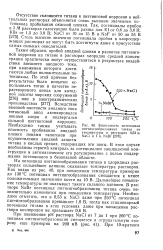 |
Зависимость потенциала питтингообразования титана от температуры в растворах 0 53 н. NaCl и 1 н. NaBr. [14] |
Таким образом, пробой анодной пленки и развитие питтинговой коррозии на титане в растворах хлоридов средней концентрации практически могут осуществляться в результате воздействия внешнего анодного тока, при наложении которого достигаются любые положительные потенциалы. [15]
Страницы: 1 2 3 4