Развитие - питтинговая коррозия
Cтраница 2
Результатом такого комбинированного воздействия может явиться не только развитие питтинговой коррозии, но и коррозионное растрескивание металла. [17]
Таким образом, пробивание анодной пленки на титане и развитие питтинговой коррозии практически могут осуществляться только в результате воздействия внешнего анодного тока, при наложении которого могут достигаться любые положительные потенциалы. По этой причине безрезультатны были попытки использовать титан в качестве нерастворимого анода для катодной защиты морских сооружений. [18]
Опубликованные за последнее время в литературе работы [1-4] объясняют механизм процесса развития питтинговой коррозии на основании теоретических представлений о щелевой коррозии. [19]
Несоблюдение хотя бы одного из указанных выше условий исключает возможность возникновения и развития питтинговой коррозии. [20]
Менее эффективен чем хроматы, но при введении в недостаточном количестве не стимулирует развития питтинговой коррозии [53], не ядовит. [21]
Менее эффективен, чем хроматы, но при введении в недостаточном количестве не стимулирует развития питтинговой коррозии [53], не ядовит. [22]
Повторные нагревы закаленных образцов сплава типа ХН65МВ с содержанием углерода более 0 01 % могут привести к развитию питтинговой коррозии в 10 % - ном растворе FeCls при 50 С. Возникновение питтингов в данном случае связывается с выделением мелкодисперсных карбидов типа МвС, богатых хромом и молибденом. [24]
Их ингибирующее действие обусловлено конкурирующей адсорбцией, в результате которой они вытесняют С1 - с поверхности и тем самым препятствуют развитию питтинговой коррозии. [25]
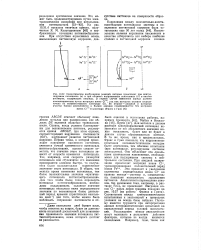
Однако, когда условия благоприятны для возникновения питтинга, реализуется кривая ABCGH, при этом отрезок, соответствующий нарушению пассивности ( GH), изображает развитие питтинговой коррозии. Первая точка, в которой происходит нарушение пассивного состояния, считается точкой критического потенциала питтингообразования, однако следует отметить, что значение этого потенциала зависит от скорости изменения потенциала. Так, например, если скорость развертки потенциала или ступенчатое его изменение производится слишком быстро, то получается более положительное критическое значение этого потенциала. [27]
 |
Сопоставление коррозионного поведения сплавов титана. [28] |
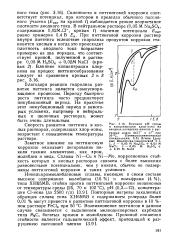
Бесспорно, ЕПК - полезная характеристика устойчивости сплавов титана, но прежде всего именно в условиях воздействия анодных токов. Пробой анодной пленки и развитие питтинговой коррозии на титане в растворах хлоридов средней концентрации практически могут наблюдаться в результате воздействия внешнего анодного тока, при наложении которого достигаются любые положительные потенциалы. [29]
 |
Установка для проведения поляризационных измерений. [30] |
Страницы: 1 2 3 4