Термохимическая величина
Cтраница 1
Термохимические величины обычно выражаются в виде стандартных теплот образования, а для большинства изученных органических соединений - стандартных теплот сгорания. Эти данные сведены в таблицы термохимических величин, которые могут применяться при расчетах теплового эффекта какой-либо реакции. [1]
Термохимические величины К, AG, A / / f, S, Cp обычно табулированы для стандартного состояния, в качестве которого, как правило, выбирается состояние идеального газа при 1 атм. Часто необходимо перейти к стандартным состояниям, выраженным в единицах концентрации. [2]
Важнейшими термохимическими величинами являются энтальпии атомизации, которые легко могут быть рассчитаны по экспериментальным теп-лотам сгорания. Благодаря тому, что теплоты сгорания измеряются в калориметрических бомбах с точностью, достигающей 0 01 - 0 02 % [3], примерно с такой же большой точностью могут быть получены и энтальпии атомизации. [3]
Все термохимические величины, кроме сродства молекулы воды к протону, известны. Поэтому, измерив потенциал появления и приняв, что продукты не несут избыточной энергии, можно рассчитать сродство к протону молекул воды. Процесс с образованием НзО может идти и иным путем, отличным от схемы ( 27), например сопровождаться дальнейшей фрагментацией радикала С2Нз или приводить к продуктам с ненулевой избыточной энергией. Поэтому целесообразно определить потенциал появления Н3О из опытов со многими соединениями, а затем отобрать такие значения сродства к протону, которые согласуются между собой. На практике количество соединений, пригодных для этой цели, ограничено имеющимися термохимическими данными. [4]
Различие термохимических величин для природной изотопной смеси водорода и для чистого протия очень мало и в данном параграфе не принимается во внимание. [5]
Определение термохимических величин химики обычно проводят при температуре 25 С. Ранее было принято называть теплоту, выделяющуюся при реакции образования данного соединения из простых веществ, теплотой образования Qf. Отрицательное значение Qf означает, что реакция образования соединения эндотермична. [6]
Получение более точных термохимических величин расширяет возможности их использования. Для расчета детонационных свойств взрывчатых веществ вполне удовлетворительной является точность в 5 - 6 ккал / моль. При оценке энергий связей, теплот атомизации, энергий напряжения, сопряжения, водородной связи и др. необходимая точность уже составляет от 2 - 3 до 0 1 - 0 2 ккал / моль. [7]
Все значения термохимических величин в таблицах выражены в ккал. [8]
В таблицах термохимических величин обычно содержатся только стандартные тепловые эффекты, относящиеся к температуре 25 С. Вместе с тем, для расчетов необходимо знать тепловые эффекты реакций при высоких температурах. [9]
Оценка погрешности принятых термохимических величин во многих случаях вызывает большие затруднения. Авторы экспериментальных работ, как правило, приводят погрешности, характеризующие случайные ошибки эксперимента. Правильно оценить эти погрешности, за редким исключением, не представляется возможным Поэтому значения погрешностей некоторых принятых в Справочнике термохимических величин ( особенно оцененных) в ряде случаев являются в какой-то мере произвольными. [10]
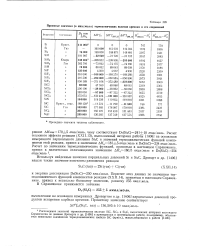 |
Принятые значения ( в кал / моль термохимических величин кремния и его соединений. [11] |
Расхождение значений термохимических величин SiC, SiCa и SiaC, вычисленных авторами настоящего Справочника по данным Дроварта и др. [1406] и приведенных в оригинальной работе, по-видимому, объясняется неверными значениями термодинамических свойств SiC ( крист. [12]
Наряду с термохимическими величинами в таблицах приводятся радиусы ионов, вычисленные либо из термохимических данных ( термохимические радиусы), либо взятые из сводки Гольдшмидта. [13]
Рассматриваемые в Справочнике термохимические величины связаны между собой. Уравнения, выражающие эту связь, основаны на законе Гесса - частном случае закона сохранения энергии. [14]
Вопрос о разделении термохимических величин на некоторые составляющие - это неоднозначная, но не термодинамическая задача. Ее решают приближенно, используя все имеющиеся физические данные. [15]
Страницы: 1 2 3 4