Термохимическая величина
Cтраница 3
Приведенные в настоящем Приложении значения термохимических величин следует использовать взамен соответствующих величин из I и II выпусков для обеспечения их согласованности с III и последующими выпусками Справочника. [31]
Целью настоящей работы является получение термохимических величин, характеризующих устойчивость некоторых хлорокомплексов переходных металлов. В литературе по этому вопросу данных недостаточно. [32]
Капустинский [75] установил, что многие термохимические величины являются линейными функциями логарифма порядкового номера элемента. [33]
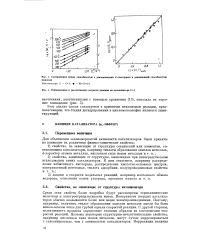 |
Наблюдаемые и рассчитанные скорости реакции на катализаторе Сг-1. [34] |
Среди этих свойств более подробно будут рассмотрены термохимические величины и электроотрицательности ионов. Поверхности твердых катализаторов обычно оказываются более или менее невоспроизводимыми. Поэтому, например, величины теплот образования окислов металлов могли бы быть использованы лишь для грубой оценки скоростей реакции. С другой стороны, селективность процесса определяют главным образом из соотношения скоростей реакций. Поэтому некоторые структурно-нечувствительные свойства, например кислотная сила ионов металлов, могут лучше коррелироваться с селективностью, чем с активностью катализаторов. [35]
Обзор литературных данных и обоснование выбора перечисленных выше термохимических величин приводятся в соответствующих параграфах глав 2 - й части I тома. В конце каждого параграфа приведены таблицы принятых значений термохимических величин. В них даны значения энергии диссоциации ( при 0 К) газообразных веществ на одноатомные газы, теплот сублимации кристаллических веществ при 0 К, энергии ионизации некоторых атомов, молекул и ионов при 0 К, теплоты образования веществ при 0, 293, 15 и 298, 15 К - В двух последних столбцах таблиц приведены значения Я [ 315 - Я иЯ2 98 15 - Н 0 соответствующих веществ. Термохимические величины, принятые в Справочнике на основании анализа литературных данных, в текстах параграфов и таблицах принятых термохимических величин выделены жирным шрифтом. [36]
Ссылка на литературу относится ко всем трем термохимическим величинам, приведенным в таблице. [37]
Таким образом теплоты образования и энтропии являются основными термохимическими величинами. [38]
Значения растворимости систем твердое тело - жидкость и термохимические величины для большинства веществ приводятся в справочной литературе. Что касается остальных данных, то, как правило, они должны предварительно определяться опытным путем. [39]
Следует отметить, что аналогичная возможность существует для оценки любой термохимической величины, входящей в выражение для теплового эффекта соответствующих реакций. Так, например, могут быть оценены величины D ( R - Н) или / ( М), если известны все остальные входящие в неравенство величины. При этом существенно знать, с потенциалом ионизации какой из молекул совпадает потенциал появления вторичного иона. Следовательно для исследований по методу ионного удара необходимо измерение потенциалов появления ионов. Методы определения их были рассмотрены выше. [40]
В настоящем параграфе не принимается во внимание разность между термохимическими величинами соединений природной изотопной смеси водорода и соединений протия, так как она значительно меньше погрешностей рассматриваемых величин. [41]
При пользовании этим способом расчета термохимических радиусов требуется, чтобы соответствующие термохимические величины были определены с достаточной степенью точности ( ошибка в определениях не должна превышать 0 3 ккал), так как приходится иметь дело с разностью теплот образования и в неблагоприятном случае возможно суммирование экспериментальных ошибок. [42]
В расчете использовались данные [4-7] по термодинамическим функциям компонентов и термохимическим величинам. [43]
Исследование термохимических свойств фторорга-нических соединений дает возможность установить закономерности в термохимических величинах и использовать их при проверке различных теорий, объясняющих особенности химических и физико-химических свойств веществ. Например, из анализа термохимических данных следует ( см. ниже), что последовательное замещение атомов водорода атомами фтора в алифатических соединениях вызывает упрочнение связи углерод - фтор. Изучение термохимических свойств фтор-производных бензола, напротив, показало, что гекса-фторбензол дестабилизирован пр сравнению с фтор-бензолом - на 38 ккал / моль. Тем не менее представляет интерес рассмотреть имеющийся экспериментальный материал с тем, чтобы выявить основные термохимические закономерности во фторор-ганических соединениях. [44]
Эти закономерности нередко использовались А. Ф. Капустинским и его учениками для приближенной оценки термохимических величин. [45]
Страницы: 1 2 3 4