Наблюдаемая разность
Cтраница 2
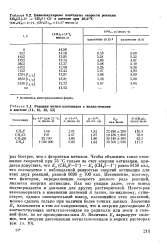 |
Бимолекулярные константы скорости реакции СН3С1 - - 1 - - СН3Г С1 - в ацетоне при 40 0 9С.| Реакции метилгалогенидов с иодид-ионами в ацетоне. [16] |
Чтобы объяснить такое отношение скоростей при 25 С только за счет энергии активации, придется допустить, что Ea ( CH3F - 1 -) - Еа ( СН31 - 1 -) равна 8150 кал, что согласуется с наблюдаемой разностью энергий активации для этих двух реакций, равной 8690 700 кал. Несомненно, поэтому, что фактором, определяющим скорость данного ряда реакций, является энергия активации. Как мы увидим далее, этот вывод подтверждается и данными для других растворителей. Некоторая закономерность в изменении значений А также, по-видимому, существует, однако окончательный вывод, касающийся этих значений, можно сделать только при наличии более точных данных. Значения Еа изменяются в том же направлении, что и энергии диссоциации D соответствующих метилгалогенидов на радикалы или ионы в газовой фазе, но не пропорциональны D. Величина Еа варьирует сильнее, чем энергии диссоциации метилгалогенидов в водных растворах ( см. гл. [17]
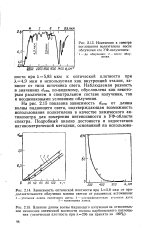
Я 4 9 мкм и используемая как внутренний эталон, зависит от типа источника света. Наблюдаемая разность в значениях с ( ОТн, по-видимому, обусловлена как некоторым различием в спектральном составе излучения, так и неодинаковыми условиями облучения. [19]
Полученные результаты ясно показывают, что в соединениях PtCl2 - 4NH3 и PtCJ2 2КС1, отвечающих одной и той же степени окисления платины, последняя имеет совершенно различную атомную рефракцию. Наблюдаемая разность далеко выходит за пределы погрешностей исследований подобного рода. Отсюда следует, что образование не разлагаемых водою комплексов в двойных и аммиачных соединениях платины проявляется весьма резко на рефрактометрических величинах. Если бы названные комплексы не существовали в растворенном состоянии, то для приведенных выше солей мы должны были бы получить одну и ту же величину для атомной рефракции платины. [20]
Сравнение значений параметров Л ( а р) ( 19з) и Л ( а) Р) 225 для полипептидов с одинаковым содержанием спиральной формы в воде и в органических растворителях показывает, что величины Л ( ар) ( ] 9з) Для органических сред больше, чем для водных растворов, а значения Л ( а, Р) 225 менее отрицательны для полипептидов в органических растворителях. Наблюдаемые разности значений параметров для двух типов растворителей имеют порядок 150 град. Так как оптическая активность п - - я - перехода имеет электростатическое происхождение [21], можно думать, что на значения Л ( а, Р) ( 19з) и Л ( а, Р) 225 влияет диэлектрическая проницаемость среды. Хотя окончательные выводы, по-видимому, делать преждевременно, возможно, что меньшее по сравнению с водными растворами левое вращение в органических растворителях обусловлено различием диэлектрических проницаемостей у этих двух типов растворителей. [21]
Статистическое решение этой задачи заключается в сравнении разности ( х-и. Если наблюдаемая разность меньше, чем рассчитанная при выбранной доверительной вероятности, считают, что нуль-гипотеза ( х и ц, неразличимы) подтверждается; тогда можно сделать вывод об отсутствии систематической ошибки в эксперименте. Наоборот, если ( х-ц) значительно больше, чем ожидаемое, или критическое, значение, можно предположить, что разность значима и допущена систематическая ошибка. [22]
Если какая-нибудь из наблюдаемых разностей превышает критическое значение или равна ему, то Я о отклоняется. [23]
Входящий в формулу ( 160) фактор ( тф / т) 1 / ( / ф / / АН) нельзя непосредственно отождествить с отношением А / А экспериментально измеряемых аррениусовских предэкспонент, поскольку, как видно из ( 161), / ф и / Ан зависят от температуры. По той же самой причине наблюдаемая разность энергий активации, Е - Е, не равна в точности разности нулевых энергий Аб0, хотя практически это различие может быть незначительным. [24]
Для рассчитанного значения t и подходящего значения у ( п - - 1) вероятность того, что разность ( т - ц) будет определенной, может быть вычислена. Чем больше значение t, тем больше вероятность того, что только большое число образцов дает реальную оценку параметров ансамбля, и что даже фактически наблюдаемая разность между результатами, полученными для двух небольших групп образцов, может не иметь никакого смысла. [25]
При этом способе измеряется изменение давления газа сначала над затемненной, а затем над освещаемой клеточной суспензией. Наблюдаемая разность давлений является результатом выделения и поглощения углекислоты и кислорода. Если дыхательный коэффициент и фотосинтетический коэффициент равны единице, то изменения давления могут быть вызваны только тем, что двуокись углерода обладает большей растворимостью в воде ( и еще большей - в щелочных растворах), чем кислород. [26]
V - Л с величиной квадратного корня из числа наблюдаемых импульсов следует, что настоящие опыты приводят к достоверным результатам. Действительно, разности 4660 и 650 соответственно в 27 и 5 5 раза больше, чем Y-N. Исключительно мало вероятно, что наблюдаемые разности обусловлены флуктуациями числа импульсов. [27]
Цианофенолы были включены в это исследование, чтобы ш-т казать, что в случае нитрофенолов большая часть АрД й действительно обусловлена стерическим ингибированием мезомерии. Поскольку циан-группа линейна, она не может быть серьезны препятствием для мезомерного взаимодействия. Небольшая, в - личина наблюдаемых разностей является серьезным доказатель / -, ством правильности предложенной интерпретации. [28]
Анализ данных, приведенных в табл. 3, показывает, что по крайней мере два полимера, поливинилдициклогексан и поли-3 - метил гексен-1, имеют аномально высокие температуры плавления. Поливинилдициклогексан плавится при 372 С, в то время как следующий член его гомологического ряда - полиаллилциклргек-сан - плавится при 230 С, так что разница температур плавления составляет 142 С. Это намного больше, чем обычно наблюдаемая разность температур плавления первого и второго членов гомологических рядов. Аномальность температуры плавления поливинил-циклогексана также видна из сопоставления его с близким по строению полимером - полистиролом, температура плавления которого равна 250 С. Можно было бы ожидать, что поливинилцикло-гексан должен плавиться при близкой температуре однако в действительности его температура плавления лежит на 120 С выше. Высшие члены гомологического ряда поливинилциклогексана плавятся примерно при тех же температурах, что и высшие члены ряда полистирола. [29]
Анализ данных, приведенных в табл. 3, показывает, что по крайней мере два полимера, поливинилдициклогексан и поли-3 - метилгексен-1, имеют аномально высокие температуры плавления. Поливинилдициклогексан плавится при 372 С, в то время как следующий член его гомологического ряда - полиаллилциклогек-сан - плавится при 230 С, так что разница температур плавления составляет 142 С. Это намного больше, чем обычно наблюдаемая разность температур плавления первого и второго членов гомологических рядов. Аномальность температуры плавления поливинил-циклогексана также видна из сопоставления его с близким по строению полимером - полистиролом, температура плавления которого равна 250 С. Можно было бы ожидать, что поливинилцикло-гексан должен плавиться при близкой температуре, однако в действительности его температура плавления лежит на 120 С выше. Высшие члены гомологического ряда поливинилциклогексана плавятся примерно при тех же температурах, что и высшие члены ряда полистирола. [30]
Страницы: 1 2 3