Простой разрыв - связь
Cтраница 2
Наряду с ионами, образующимися при простом разрыве связей, в масс-спектрах почти всех молекул, содержащих более двух углеродных атомов, присутствуют ионы, возникновение которых связано с перегруппировкой атомов в момент диссоциации. Особенно часто наблюдаются перегруппировки с миграцией атома водорода, как этого и следовало ожидать в связи с его малой массой. В некоторых случаях, как, например, в случае образования иона с массой 43 в масс-спектре неогексана ( СН3) 3С - СН2 - СН3, наличие перегруппировки не вызывает сомнения. Образующемуся иону отвечает формула С3Н, и его возникновение, следовательно, должно включать миграцию водородного атома, а также разрыв по меньшей мере двух С-С связей. [16]
При другом подходе к интерпретации реакций с простым разрывом связи используется представление о локализации заряда в молекулярных ионах как о движущей силе реакции. [17]
Для перегруппировки, так же как и для простого разрыва связей, необходимо, чтобы на данной связи или группе связей сконцентрировалась энергия, достаточная для осуществления процесса. Трактовать эту энергию как энергию активации можно без оговорок только в случае статистических механизмов, так как само понятие энергии активации предполагает статистическое распределение молекул по величине тепловой энергии. [18]
Миграция водорода энергетически более выгодна по сравнению с простым разрывом связи без миграции, так как она приводит к образованию двойной связи; с каждой разорванной связью образуется новая. Атом водорода мигрирует из Р - ПОЛОЖСНИЯ к разрываемой связи. Наличие в цепи атома кислорода или азота в а-положении к разрываемой связи увеличивает вероятность данной перегруппировки, очевидно, благодаря наличию у них несвязанных электронов. При введении кислорода ( фе-нилэтиловый эфир) пик соответствующего перегруппировочного иона с массой 94 становится максимальным в спектре. В случае наличия сильного электроотрицательного заместителя и а-атома кислорода или азота ( амиды, карбонаты, фосфаты и так далее) может осуществляться перегруппировка с миграцией двух атомов водорода. [19]
Обычно считают, что локализация катион-радикального центра на азоте инициирует простые разрывы связей С-С рядом с гетероатомом, что приводит к стабильным аммониевым ионам. Нужно, однако, помнить, что именно высокая устойчивость последних ионов является движущей силой распада, а не локализация заряда в М на азоте, так как ионизация осуществляется за счет удаления электрона с делокализованной молекулярной орбитали. [20]
Процессы типа ( 3.1, а) чаще всего предполагают простой разрыв связей, в отличие от второго механизма распада, который сопровождается перегруппировками с миграцией атомов водорода или ( реже) других фрагментов. Процессы образования менее стабильных катион-радикалов ( б) в совокупности с нейтральными частицами в некоторых случаях могут быть более энергетически выгодными, чем процессы образования более устойчивых катионов ( а) в сочетании с радикалами. Вследствие этого относительный вклад процессов типа ( 3.1 б) в общий ионный ток осколочных ионов приуменьшении энергии ионизации может возрастать. Этой особенностью фрагментации нередко пользуются для выявления пиков перегруппировочных ионов в спектрах. [21]
Перегруппировочные ионы представляют собой осколки, происхождение которых нельзя описать простым разрывом связей в молекулярном ионе. Они получаются в результате внутримолекулярной атомной перегруппировки в процессе фрагментации Особенно широко распространены перегруппировки, включающие миграцию атомов водорода в молекулах, содержащих гетероатом. [22]
He может опровергнуть очевидного положения, что этил-катион образуется По механизму простого разрыва связи. [23]
Автор показывает возможности низковольтной масс-спектрометрии для дифференциации перегруппировочных процессов и распадов с простым разрывом связей. В книге рассматриваются также новые методы масс-спектрометрии: ионизация полем, химическая ионизация и спектроскопия ионного циклотронного резонанса. [24]
Масс-спектры алкилциклановых углеводородрв характеризуются большей специфичностью, так как возможность образования стабильного иона путем простого разрыва связи имеется лишь при отщеплении алкильного заместителя. [25]
Образование отрицательных ионов происходит в области энергии электронов ( 8 эВ) при простом разрыве связей; электрон присоединяется к фрагменту, содержащему двойную связь. [26]
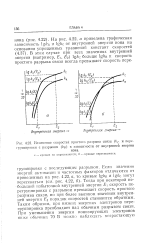 |
Изменение скоростей простого разрыва связи ( kc и перегруппировки с разрывом ( & R в зависимости от внутренней энергии. [27] |
Тогда при некоторой небольшой избыточной внутренней энергии EI скорость перегруппировки с разрывом превышает скорость простого разрыва связи, но при более высоком значении внутренней энергии Е2 порядок скоростей становится обратным. Таким образом, при низких энергиях электронов перегруппировка преобладает над обычным разрывом связи. [28]
Накопление экспериментальных данных по взаимодействию сложных органических молекул с ионизирующими электронами показало, что предположение о преимущественно простом разрыве связей в процессе диссоциативной ионизации не находит подтверждения. [29]
Ионы могут перестраиваться до или в ходе распада, давая продукты, которые не образуются в результате простого разрыва связей исходного иона. [30]
Страницы: 1 2 3 4