Распад - последнее
Cтраница 3
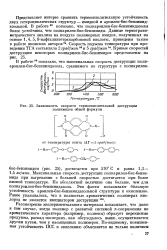 |
Зависимость скорости термоокислительной деструкции полиимидов общей формулы. [31] |
Рассмотрение экспериментального материала показывает, что даже в том случае, когда полимер с развитой системой зт-сопряжения не ароматического характера ( например, полиены) образует перекисные продукты, распад последних, как обсуждалось выше, осуществляется другим путем, чем у насыщенных полимеров. [32]
Внесение уксусной кислоты и ее зфиров, ведущее к увеличению антидетонационной эффективности ТЭС, объясняется образованием в условиях двигателя тетраацетата свинца РЬ ( СНзСОО) 4, взаимодействие которого с гидроперекисями сводится к быстрому и глубокому распаду последних. [33]
Современное представление о механизме явлений в анодном процессе при применении угольного анода исходит из того, что процесс горения состоит из стадий химической адсорбции кислорода на угле, образования промежуточных углерод-кислородных соединений типа СЛОУ, распада последних на СО и С02 и десорбции этих газов с поверхности анода. [34]
Лев пытается объяснить синтез белковых веществ в растениях, исходя из твердо установленного физиологическими опытами факта, что аспарагин образует основное ядро, которое либо является исходным для построения молекулы белка, либо встречается в продуктах распада последнего. Согласно Леву, активным ядром белка является не сам аспарагин, а его гипотетический альдегид. [35]
Распад последних на атомы фосфора наступает выше 2500 С. [36]
Как указывалось выше, основным актом продолжения цепи является взаимодействие олефинового радикала общего вида R CHGHCHR с кислородом с образованием соответствующего перекисного радикала. Распаду последнего предшествует изомеризация, которая может происходить по двум направлениям. [37]
Взаимодействие с растворителем растворенного вещества может вызвать распад последнего на ионы. Распад растворенного вещества на ионы под действием молекул растворителя называется электролитической диссоциацией или ионизацией веществ в растворах. [38]
Наконец, изменение скорости тиурамной вулканизации [79] в присутствии таких соединений, как тиомочевина ( слабый нуклеофил) или меркаптобензотиа-зол и нафтил-2 - тиол ( слабые кислоты), не обязательно свидетельствует о ее ионном механизме. Тиурам является аналогом ацильных перекисей, а распад последних по радикальному механизму, как известно [83], ускоряется в присутствии аминов. С другой стороны, меркаптобензотиазол и тионафтол могут ингиби-ровать радикальные процессы. [39]
Для разных соединений ДЩ лежит в пределах 250 - 380 кДж / моль, ДЯ - в пределах 85 - 1.40 кДж / моль, что обеспечивает возможность заселения триплетных ( ТЕ, 250 330 кДж / моль) и синглетных [ SE. Сравнение 1 2-диоксетанов с а-лакто-нами показывает, что распад последних значительно более экзотермичен. [40]
В воздухе превращение протекает столь разрушительно, что оно названо чумой; в инертной же атмосфере распад не происходит. Поэтому добавление тугоплавкого силикатного стекла к порошку дисилицида молибдена ослабляет распад последнего. [41]
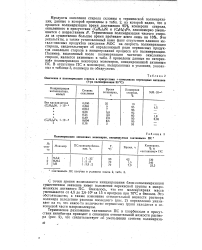 |
Полимеризация виниловых мономеров, инициируемая активным ПС. [42] |
Оказалось, что его молекулярная масса уменьшается от 4 5 до 2 6 - 10s за 15 ч прогрева при 70 С в бензоле. Это обстоятельство, а также изменение относительной вязкости раствора полимера вследствие распада последнего ( рис. 2) определенно указывает на то, что какое-то количество перекисных групп находится в неконцевой части макромолекулы. [43]
Соотношение между обоими путями обмена зависит от упомянутых выше свойств атома X в данном соединении. Обмен в сильных кислотах, способных давать орто-формы, должен идти через распад последних на кислоту и воду, тогда как в слабых кислотах возможен второй путь распада. В таких случаях склонность к обмену симбатна склонности к гидролизу. [44]
Соотношение между обеими путями обмена зависит от упомянутых выше свойств атома X в данном соединении. Обмен в сильных кислотах, способных давать орто-формы, должен идти через распад последних на кислоту и воду, тогда как в слабых кислотах возможен второй путь распада. В таких случаях склонность к обмену симбатна склонности к гидролизу. [45]
Страницы: 1 2 3 4