Распад - гидроперекись
Cтраница 1
Распад гидроперекисей кумила, тетралила и трет. [1]
Распад гидроперекиси в тетралине в атмосфере азота протекает, по-видимому, цепным путем. [2]
Распад гидроперекисей может быть вызван повышением температуры, присутствием некоторых металлов переменной валентности, преимущественно Fe, Co, Cu, Mn, Sn, и, наконец, некоторыми накопляющимися непосредственно в зоне реакции кислыми продуктами. В углеводородной среде наиболее частыми инициаторами распада гидроперекисей являются железо и его окислы, всегда присутствующие в нефтяных дистиллятах и топливах, а также накапливающиеся соединения с карбоксильной группой, в том числе карбоновые кислоты, оксикислоты. [3]
Распад гидроперекиси под действием NO и света приводит к ускорению деструкции ПС. [4]
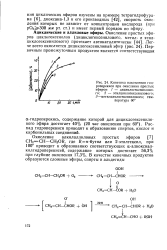 |
Кинетика накопления гидроперекиси при окислении простых эфиров. / - дициклогексенилово-го. 2 - этилциклогексенилового. 3-метилциклогексенилового. температура 60. [5] |
Распад гидроперекиси приводит к образованию спиртов, кислот и карбонильных соединений. [6]
Распад гидроперекисей, образующихся при окислении углеводородов, в радиационно-химических процессах при низких и средних температурах приводит к образованию диалкилперекисей и спиртов, карбонильные соединения не образуются. Термический и радиационно-термический распады гидроперекисей сопровождаются образованием карбонильных соединений и спиртов. Процессы радиационно-химического окисления в жидкой фазе изучены главным образом на примерах окисления углеводородов различного строения. [7]
Распад гидроперекиси в тетралине в атмосфере азота протекает, по-видимому, цепным путем. [8]
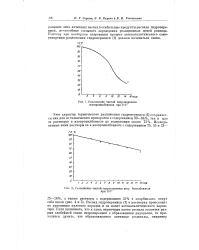 |
Разложение чистой гидроперекиси изопропилбензола при 110. [9] |
Распад гидроперекиси ( I) в растворах происходит по уравнению нулевого порядка и не носит автокаталитического характера. [10]
Распад гидроперекиси происходит в водной щелочной среде с заметно большей скоростью, чем в углеводородной среде. Соответствующие данные приведены в таблице. [11]
Распад гидроперекисей на неактивные продукты характерен для ряда соединений, содержащих некоторые элементы V и VI групп. Такими соединениями являются, в частности, диалкилселе-ниды. Нередко в одном соединении сочетаются два стабилизирующих элемента: сера и фосфор. [12]
Некатализируемый распад гидроперекиси кумила в этих условиях протекает с неизмеримо малой скоростью. Распад гидроперекиси с образованием молекулярных продуктов отсутствует. [13]
Механизм распада гидроперекисей, приводящий к образованию радикалов, еще окончательно не установлен. [14]
После распада гидроперекиси молекула лавсана распадается. [15]
Страницы: 1 2 3 4