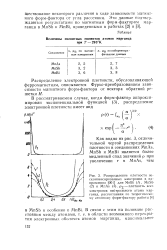
Распределение - электронная плотность
Cтраница 1
Распределение электронной плотности в исходной нере-агирующей молекуле ( статический фактор) под воздействием электрофильного агента может значительно изменяться ( динамический фактор), что также повлечет за собой изменение скорости и направления реакции. [1]
 |
Схема переходов и числа заполнения. [2] |
Распределение электронной плотности в пространстве вблизи данного ядра зависит от характера химической связи. В связи с этим постоянная экранирования для одинаковых ядер будет различна в разных химических соединениях. Изменение частоты резонанса в зависимости от характера химической связи носит название химического сдвига. [3]
Распределение электронной плотности для кристалла [ см. (1.21) ] можно построить, если кроме индексов интерференции известны знаки и значения структурных амплитуд Fhki - Структурные амплитуды связаны с интенсивностью дифракционных рефлексов, которая определяется экспериментально из рентгенограммы. [4]
Распределение электронной плотности между атомом металла и лигандом зависит от природы металла, степени его окисления и от строения орг. При этом изменения результирующих зарядов на атоме металла и лиганде при образовании я-связи невелики, что обусловлено особенностями связей металл - лиганд. Эти связи состоят из двух компонент: донорно-акцепторной и дативной. Первая обусловлена подачей я-электронов лиганда на мол. Вторая включает обратную подачу электронов металла на мол. [5]
Распределение электронной плотности в облаках с / 1 в ряду nd -, / - облаков и других еще более сложно, чем в ряду np - облаков. Однако закономерность в изменении количества максимумов и минимумов в ходе кривой 4nr - [ R ( r) ] - г в любом данном ряду / - облаков сохраняется такой же, как и в ряду np - облаков. С каждым следующим значением п в ряду состояний с данным / число максимумов радиальной вероятности увеличивается на единицу. [6]
Распределение электронной плотности в молекуле зависит не только от характера отдельных связей в ней ( as s, s - p, GJI-P, ЯР - И пр. Определенное взаимное расположение связывающих электронных облаков - направленность химической связи - приводит к определенному расположению в пространстве ядер химически связанных атомов, к определенному ядерному скелету данной молекулы. ТВС позволяет объяснять и предсказывать пространственные структуры многих молекул, исходя из электронных структур атомов, составляющих молекулы. [7]
Распределение электронной плотности в молекуле пиридина подтверждается тем, что пиридин менее реакционно-способен, чем бензол, и заместители при проведении реакций электро-фильного замещения, даже таких реакций, при которых исключается предварительное протонирование атома азота, направляются, как и в нитробензоле, в - положение относительно атома азота, а нуклеофильные реагенты ( например, амид натрия) замещают атомы водорода в ее - и f - положениях. [8]
Распределение электронной плотности в бинарных полупроводниках с тетраэдрическими связями рассматривается в рамках дисперсионной теории. Сравнением теоретических и экспериментальных факторов рассеяния рентгеновских лучей в кристаллах арсенида галлия найдены параметры химической связи: параметр переноса заряда, величина смещения зарядов связи из середины ковалентной связи, эффективные заряды атомов галлия и мышьяка, а также факторы Дебая - Уолле-ра для атомных зарядов и заряда связи. [9]
Распределение электронной плотности, обусловливающей ферромагнетизм, описывается Фурье-преобразованием зависимости магнитного форм-фактора от вектора обратной решетки Я. [11]
Распределение электронной плотности будет симметричным по отношению к направлению связи, если она осуществляется электронами s - оболочки, как это наблюдается в молекуле водорода. [12]
Распределение электронной плотности, получаемое по РМХ для кластера С3з ковалентного кристалла алмаза, совершенно не соответствует действительному; заряды на атомах принимают значения от 0 38 на центральном атоме до - 0 76 на краевых, проходя через значения 0 37, 0 17, 0 06 для промежуточных атомов. [13]
Распределение электронной плотности в молекуле водорода имеет принципиальное значение для теории ковалентной связи. [14]
Распределение электронной плотности в изолированной молекуле и в реакционном комплексе, особенно образованном при участии энергично действующего электронодонорного или электроноакцепториого реагента, различно вследствие эффекта поляризации молекулы. Его роль может быть выявлена, если перейти от полярных молекул органических веществ, о реакциях которых говорилось выше, к молекулам неполярным и притом легко поляризующимся. [15]
Страницы: 1 2 3 4