Раствор - сильный электролит
Cтраница 1
Растворы сильных электролитов сохраняют высокую электропроводность даже при очень больших концентрациях. Электропроводность растворов слабых электролитов быстро падает с увеличением концентрации. [1]
Раствор сильного электролита отличается по своим свойствам от идеального раствора, что обусловлено электростатическим взаимодействием между ионами. [2]
Растворы сильных электролитов ( солей, сильных кислот и сильных оснований) не подчиняются закону действия масс. В их растворах находятся только катионы и анионы данного растворенного вещества и практически нет недиссоциированных молекул этого вещества. Но экспериментально определенная степень диссоциации сильных электролитов очень невелика. Закон действия масс выведен без учета действия сил притяжения и отталкивания между ионами растворенного вещества и молекулами растворителя. Эти силы особенно заметны в растворах сильных электролитов, где все молекулы растворенного вещества диссоциированы на ионы, несущие разноименные электрические заряды. В концентрированных растворах слабых электролитов также наблюдаются отступления от закона действия масс, потому что в них концентрация электрически заряженных компонентов раствора значительно больше, чем в разбавленных растворах. По теории растворов сильных электролитов при повышении концентрации растворов подвижность ионов в растворе уменьшается под влиянием взаимодействия ионов, так как среднее расстояние между ионами уменьшается. [3]
Растворы сильных электролитов хорошо проводят электрический ток, растворы слабых электролитов - плохо. [4]
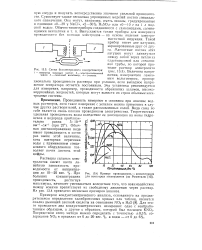 |
Схема безэлектродного кондуктометра.| Кривые проводимость - концентрация для некоторых электролитов ( по Розенталю. [5] |
Растворы сильных электролитов имеют почти линейную зависимость проводимости от концентрации до 10 - 20 вес. [6]
Растворы сильных электролитов отличаются от растворов слабых электролитов тем, что в них нет недиссоциированных молекул. Это подтверждается современными физическими и физико-химическими исследованиями. Например, исследование кристаллов сильных электролитов типа КС1 рентгенографическим путем подтверждает тот факт, что кристаллические решетки солей построены из ионов. [7]
Растворы сильных электролитов при больших концентрациях обладают значительной электропроводностью, причем она с разбавлением растворов возрастает незначительно. Растворы слабых электролитов при больших концентрациях отличаются незначительной электропроводностью, сильно увеличивающейся при разбавлении растворов. [8]
Растворы сильных электролитов отличаются от растворов слабых электролитов тем, что в них нет недиссоциированных молекул. Это подтверждается современными физическими и физико-химическими исследованиями. [9]
Назовите растворы сильных электролитов, которые существуют в природе. [10]
 |
Зависимость эквива. [11] |
Теория растворов сильных электролитов показывает, что особенности сильных электролитов обусловлены наличием электростатического взаимодействия между ионами. Взаимное притяжение между ионами в растворах ведет к образованию ионных атмосфер. Может возникнуть предположение, что движение ионов сильного электролита затрудняется ионными атмосферами. Но предположение, что ион, двигаясь в растворе, перемещается вместе со своей ионной атмосферой, является ошибочным уже потому, что приводит к противоречию с опытом. [12]
 |
Диссоциация КС1 при 18. [13] |
Неподчинение растворов сильных электролитов закону действия масс, находящееся в резком противоречии с классической теорией электролитической диссоциации Аррениуса, долгое время не находило удовлетворительного объяснения. [14]
Неподчинение растворов сильных электролитов закону действия масс, находящееся в резком противоречии с классической теорией электролитической диссоциации Аррениуса, долгое время не находило удовлетворительного объяснения. В настоящее время оно объясняется с точки зрения так называемой теории сильных электролитов, введенной в науку Дебаем и Гюккелем в 1923 г. В экспериментальной проверке и дальнейшем развитии этой теории видная роль принадлежит В. К - Семенченко, А. И. Бродскому, В. А. Плескову и др. Ввиду математической сложности теории сильных электролитов о ней можно дать здесь лишь самое общее представление. [15]
Страницы: 1 2 3 4