Разбавленный раствор - неэлектролит
Cтраница 1
Разбавленные растворы неэлектролитов обладают. [1]
Разбавленные растворы неэлектролитов обладают рядом свойств ( коллигативные свойства), количественное выражение которых зависит только от числа находящихся в растворе частиц растворенного вещества и от количества растворителя. Некоторые коллигативные свойства растворов используются для определения молекулярной массы растворенного вещества. [2]
Свойства разбавленных растворов неэлектролитов, относящихся к нелетучим веществам, описываются следующими законами. [3]
Для разбавленного раствора неэлектролита, согласно ( 103) ( гл. [4]
Поведение разбавленных растворов неэлектролитов как идеальных разбавленных растворов обусловливает их так называемые общие свойства растворов, которые не зависят от природы растворенного вещества, а только от его долевой мольной концентрации. [5]
Для разбавленных растворов неэлектролитов все эти величины находятся в простой пропорциональной зависимости от числа молекул растворенного вещества. [6]
В разбавленном растворе неэлектролита число частиц совпадает с числом молекул, в то время как в разбавленном растворе электролита число частиц увеличивается в результате диссоциации и во столько же раз возрастает депрессия. [7]
В умеренно разбавленных растворах неэлектролитов коэффициент активности заметно отличается от единицы. [8]
В разбавленных растворах неэлектролитов молекулы растворенного вещества практически не взаимодействуют друг с другом из-за большого расстояния между ними. Поведение этих молекул в растворе аналогично поведению молекул идеального газа. Если, например, налить в стакан концентрированный раствор сахарозы, а сверху слой чистой воды, то через некоторое время концентрация молекул сахарозы станет одинаковой во всем объеме раствора. Такое взаимное проникновение молекул называется диффузией. В данном случае имеет место встречная, или двусторонняя, диффузия молекул сахарозы в воду и молекул воды в сахарозу. [9]
В разбавленных растворах неэлектролитов молекулы растворенного вещества практически не взаимодействуют друг с другом из-за большого расстояния между ними. Поведение этих молекул в растворе аналогично поведению молекул идеального газа. Действительно, если, например, налить в стакан концентрированный раствор сахарозы, а сверху слой чистой воды, то через некоторое время концентрация молекул сахарозы станет одинаковой во всем объеме раствора. Такое взаимное проникновение молекул называется диффузией. В данном случае имеет место встречная или двусторонняя диффузия молекул сахарозы в воду и молекул воды в сахарозу. [10]
Исследование свойств разбавленных растворов неэлектролитов показало, что понижение давления пара, повышение температуры кипения и понижение температуры замерзания обусловлены только числом растворенных частиц в определенном объеме данного растворителя и не зависят от природы растворенного вещества. В этом заключается сущность законов Рауля. [11]
Некоторые свойства разбавленных растворов неэлектролитов могут быть описаны количественно и выражены в виде законов. [12]
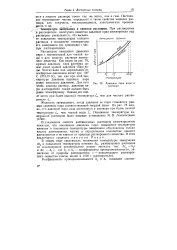 |
Давление пара воды и раствора. [13] |
Исследование свойств разбавленных растворов неэлектролитов показало, что понижение давления пара, повышение температуры кипения и понижение температуры замерзания обусловлены только числом растворенных частиц в определенном количестве данного растворителя и не зависят от природы растворенного вещества. В этом заключается сущность законов Рауля. [14]
Некоторые свойства разбавленных растворов неэлектролитов могут быть описаны количественно и выражены в виде законов. [15]
Страницы: 1 2 3 4